Kronisk njursjukdom och kronisk njursvikt har uppmärksammats som ett potentiellt folkhälsoproblem på många håll i världen.
Utöver risken att drabbas av kronisk njursvikt har studier visat att risken för kardiovaskulär sjukdom är i paritet med den vid diabetes eller hypertoni.
Kritiker hävdar att en utbredd användning av olika formler för att uppskatta den glomerulära filtrationshastigheten kan leda till en överskattning av det potentiella folkhälsoproblemet, och att risken för en »epidemi« av kronisk njursvikt är överdriven, särskilt hos äldre.
Mätningar av eGFR kompletterat med bedömning av andra riskfaktorer kan troligen identifiera dem som har risk för en snabbare progress av sin njursjukdom, vilket kan kräva ett mer selekterat medicinskt omhändertagande.
Screening i syfte att tidigt identifiera och behandla patienter med lätt till måttlig njursjukdom bör fokuseras på högriskpopulationer.
Under det senaste decenniet har kronisk njursjukdom och kronisk njursvikt uppmärksammats som ett potentiellt folkhälsoproblem på många håll i världen. Förekomsten av njursjukdomar har ökat av flera skäl, bland annat av att allt fler blir äldre och drabbas hjärt–kärlsjukdom, hypertoni och typ 2-diabetes. Flera studier har visat att prevalensen av kronisk njursjukdom i befolkningen är så hög som upp till ca 15 procent eller mer i länder som Norge, England, USA, Kina, Kanada, Australien och Japan. Incidensen av terminal kronisk njursvikt med behov av dialys eller njurtransplantation har också ökat på många håll i världen. Detta innebär att omhändertagandet av patienter med kronisk njursjukdom är, och kommer att bli, en stor hälsoekonomisk utmaning för många länder [1].
En av orsakerna till att kronisk njursjukdom fått större uppmärksamhet är möjligheten att på ett enkelt sätt uppskatta den glomerulära filtrationshastigheten (estimerad GFR, eGFR) från koncentrationen av serumkreatinin med olika ekvationer som inkluderar parametrar som ålder, kön, etnicitet, kroppsvikt och muskelmassa. Detta har bidragit till att många individer med normalt eller nära normalt serumkreatinin klassificeras till något stadium av kronisk njursjukdom. Eftersom njursjukdom är vanligare än man tidigare trott argumenterar många för att särskilda åtgärder för tidig upptäckt och behandling bör sättas in för att bromsa försämringen av njurfunktionen, medan andra tvärtom hävdar att de nya formlerna för uppskattning av eGFR överskattar problemets omfattning.
Definition av kronisk njursjukdom
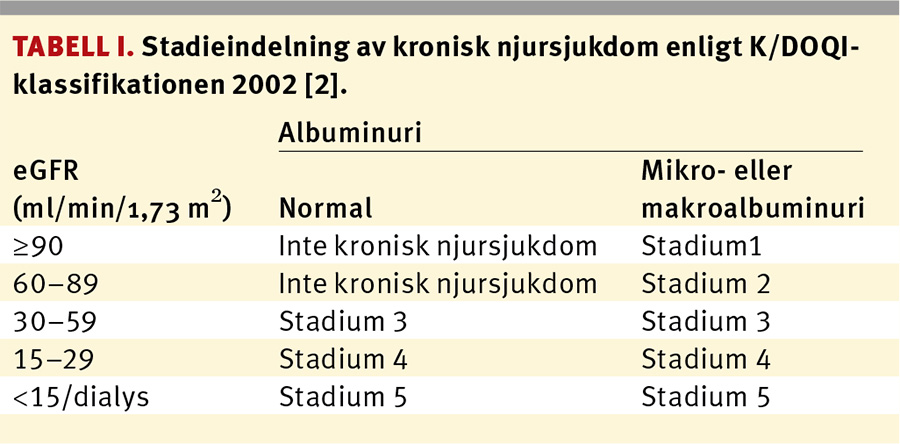
För cirka tio år sedan föreslogs i riktlinjer från Kidney Disease Outcomes Quality Initiative (K/DOQI) i USA en stadieindelning av kronisk njursjukdom som fick snabb spridning (Tabell I) [2]. Stadieindelningen har använts i populations-, observations- och interventionsstudier, men har också fått kritik. Enkelheten är den stora fördelen, eftersom eGFR mäts på ett enkelt sätt från kreatinin i serum med den s k MDRD-formeln (Modification of diet in renal disease). Syftet med riktlinjerna var att underlätta tidig identifiering av patienter med njursjukdom som har risk för ytterligare njurfunktionsförsämring och som därmed är i riskzonen för att utveckla terminal kronisk njursvikt med behov av dialys eller transplantation.
Formeln används numera också för att uppskatta risken för framtida hjärt–kärlsjukdom hos individer med nedsatt njurfunktion. Patienter med njursjukdom under minst tre månader, och som antingen har eGFR på mindre än 60 ml/min/1,73 m2 eller andra tecken på njurskada, som albuminuri, hematuri eller ultraljudsförändringar ingår i klassifikationen (Tabell I).
Mätning och uppskattning av GFR
Definitionen av normal eller onormal njurfunktion är inte tydlig. Vissa anser att skillnaden är den GFR-nivå då njurarna inte längre kan upprätthålla normal elektrolytbalans eller vätskehomeostas, och då risken för sekundära komplikationer relaterade till inkomplett njurfunktion uppträder, dvs renal anemi, metabol acidos och tecken till sekundär hyperparatyreoidism. Denna indelning är emellertid inte användbar i klinisk praxis eftersom njurarna har en stor förmåga att upprätthålla normal elektrolytbalans och vätskehomeostas över ett brett område av glomerulär filtration. Det mest tillförlitliga sättet att mäta GFR är att bestämma clearance för olika filtrationsmarkörer. Eftersom dessa metoder är både dyra och tidskrävande har de ersatts av olika formler som uppskattar GFR utifrån koncentrationen av kreatinin i blodet, korrigerat för ålder, vikt, kön, etnicitet mm (t ex Cockcroft–Gault och MDRD).
För att öka tillförlitligheten i att utifrån ett kreatininvärde prediktera risken för fortsatt njurfunktionsförsämring, eller risken för framtida kardiovaskulär sjukdom, kan graden av albuminuri adderas till dessa formler för att förstärka deras värde. I den prospektiva kohortstudien REGARDS (Reason for geographic and racial differences in stroke) ingick 26 643 vuxna personer under åren 2003–2010. Deltagarna delades in i åtta grupper definierade med eGFR bestämt utifrån deras serumkreatinin, cystatin C eller grad av albuminuri. Patienterna följdes under sex år och man fann att tillägg av cystatin C till serumkreatinin och urinalbumin förbättrade det prediktiva värdet för mortalitet av alla orsaker och även värdet för risken för terminal njursvikt med behov av dialys eller transplantation [3].
Förekomst av kronisk njursjukdom
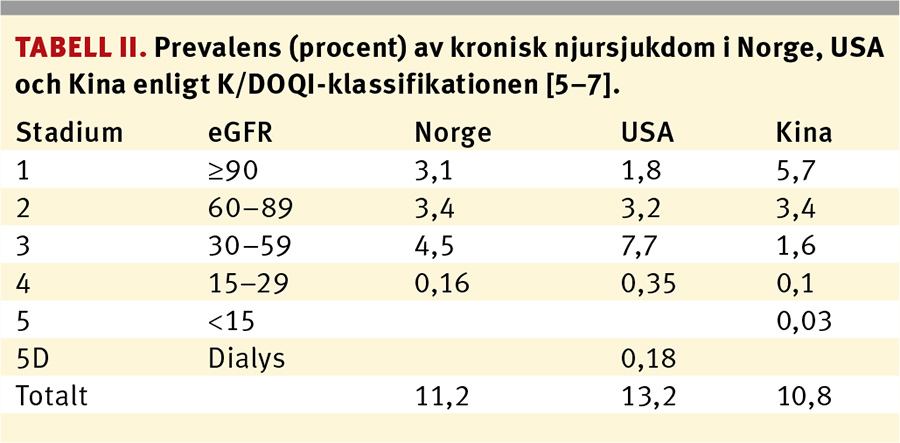
När man i den norska HUNT 2-studien använde den stadieindelning som föreslagits av K/DOQI fann man att prevalensen av kronisk njursjukdom i en population på 65 181 individer i Nord-Trøndelag (71 procent av befolkningen över 20 års ålder) var cirka 11 procent (Tabell II) [4]. En undersökning av prevalensen i Sverige visade att ca 4,3 procent av 571 000 individer hade ett eGFR (MDRD) mindre än 60 ml/min/1,73 m2 [5]. Andra studier har visat att prevalensen av kronisk njursjukdom i USA ökade från ca 10 till ca 13 procent i början av 2000-talet (Tabell II). Prevalensen har ökat på ett liknande sätt i Taiwan, Japan, Centralamerika och i många andra länder det senaste decenniet. Tillsammans indikerar dessa höga och ökande prevalenssiffror att jordens befolkning står inför en »epidemi« av kronisk njursjukdom [1].
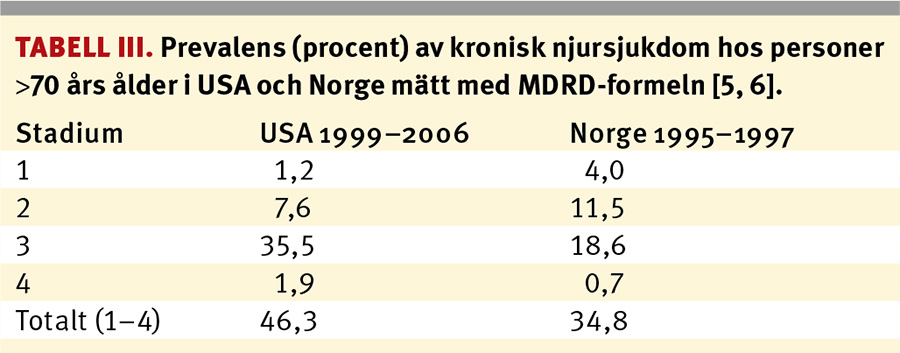
Om man därutöver säranalyserar olika åldersgrupper finns studier som visar att cirka 23–36 procent av befolkningen över 64 års ålder i västvärlden har något stadium av kronisk njursjukdom. Den högsta prevalensen av kronisk njursjukdom har rapporterats hos individer över 70 år i USA, där upp till 38 procent har kronisk njursjukdom stadium 3 eller 4 (Tabell III) [6]; en viktig upplysning eftersom 16 procent av befolkningen i USA är 60 år eller äldre. En undersökning från Kina visar att av 47 204 individer hade 10,8 procent något stadium av kronisk njursjukdom (Tabell II) [7]; 1,7 procent av populationen hade ett eGFR mindre än 60 ml/min/1,73 m2 och 9,4 procent hade albuminuri.
Antalet individer med kronisk njursjukdom i Kina kan uppskattas till cirka 119 miljoner. I vissa regioner i Kina har 18,3 procent av populationen kronisk njursjukdom i något stadium [7]. Om GFR mäts med cystatin C är dock prevalensen för kronisk njursjukdom lägre än med MDRD-formeln. Således finns en risk för att den epidemi vi talar om delvis kan vara beroende av det sätt med vilket vi uppskattar GFR.
Kronisk njursjukdom hos äldre
Prevalensen av kronisk njursjukdom i den äldre befolkningen är hög. I t ex USA, Norge och Kina har 46 , 35 respektive 28 procent av äldre individer kronisk njursjukdom i något stadium enligt K/DOQI-definitionen (Tabell III). Även om en stor andel patienter med terminal njursvikt med behov av dialys och njurtransplantation kommer från denna grupp är det uppenbart att risken för progress till terminal njursvikt hos äldre patienter med njursjukdom är relativt liten, lägre än vad som tidigare antagits. Detta har gett upphov till en livlig debatt om huruvida stadieindelningen av kronisk njursvikt är lämplig att använda hos äldre, eftersom den kan felklassificera äldre individer med ett lågt GFR som egentligen är normalt och beror på en nedsättning av njurfunktionen i relation till hög ålder.
Medel-GFR hos en grupp friska personer över 80 år i Italien var 84 ml/min/1,73 m2 och den onormala nedre gränsen (definierad som –2 standarddeviationer) var 52 ml/min/1,73 m2 [8]. Således sjunker GFR utan några kliniskt relevanta konsekvenser hos friska äldre individer. Den normala njurfunktionen hos äldre kan vara lägre än 60 ml/min, d v s under den nedre gräns som föreslagits i K/DOQI-klassifikationen.
En metaanalys av mer än två miljoner personer från olika världsdelar visade att lågt eGFR och ökad albuminuri är associerat med ökad risk för mortalitet och utveckling av allvarlig njursvikt oavsett ålder [9]. Samma studie stödjer användandet av K/DOQI-klassifikationens stadieindelning av njurfunktionsnedsättning i kombination med förekomst av albuminuri, oavsett åldersgrupp.
Överskattning av folkhälsoproblemet?
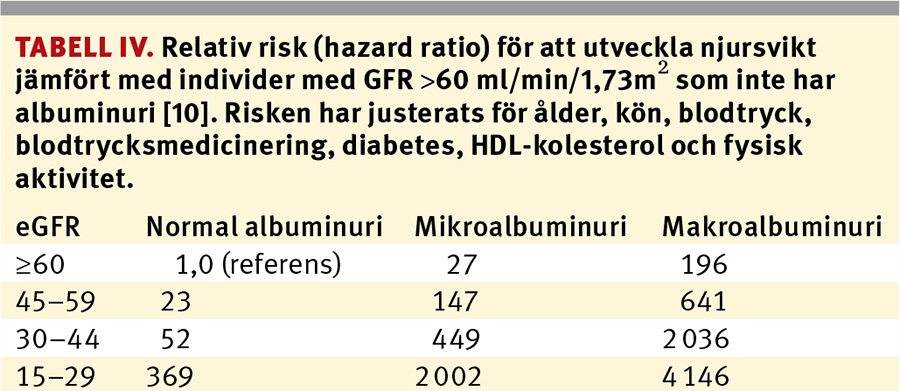
Även om många förespråkar användning av kreatininbaserade formler för uppskattning av GFR finns många kritiker och tvivlare som hävdar att en alltför utbredd användning av dessa formler kan leda till en överskattning av det potentiella hälsoproblemet. Många förespråkar därför en mer precis definition av kronisk njursvikt och att t ex utsöndringen av albumin i urinen bör vara en kompletterande parameter i stadieindelningen (Tabell IV) [10]. Många studier har visat att pro-gresstakten av njursvikt är korrelerad till graden av albuminuri.
MDRD-formeln kanske också överskattar frekvensen av kronisk njursjukdom hos kvinnor, eftersom de har mindre muskelmassa. Flera studier har visat att kvinnor utgör en stor andel av patienter med kronisk njursjukdom i stadium 3. I USA var den uppskattade prevalensen högre hos kvinnor än hos män. I den norska HUNT 2-studien var majoriteten av personerna med kronisk njursjukdom i stadium 3 kvinnor, och de flesta var över 70 år. Detta står i stark kontrast till den könsrelaterade förekomsten av terminal njursvikt. Incidensen av kronisk njursvikt med behov av dialys är ca 30 procent högre hos män än hos kvinnor.
Progress av kronisk njursjukdom
Risken för terminal njursvikt ökar med minskande GFR och ökande albuminuri, oberoende av varandra. I HUNT 2-studien fann man att eGFR och albuminuri var de två viktigaste faktorerna som predikterade utveckling av njursvikt, efter justering för andra riskfaktorer [10]. Ålder, kön, hypertoni, diabetes och andra kardiovaskulära riskfaktorer adderade inte till det prediktiva värdet.
Trots att prevalensen av kronisk njursvikt i stadium 3 har rapporterats vara hög är frekvensen av personer med kronisk njursjukdom i stadium 4 och 5 låg i befolkningen (Tabell II och III). Prevalensen av kronisk njursjukdom stadium 4 var i en av de senaste rapporterna från USA 0,35 procent (22 gånger lägre än för stadium 3), och för kronisk njursvikt i stadium 5 var den 0,11 procent. En vanlig förklaring till de låga frekvenstalen av stadium 4 och 5 är att individer med stadium 3 ofta avlider i hjärt–kärlsjukdom innan de når stadium 4 eller 5. Det finns dock studier som visat att individer över 70 års ålder med kronisk njursjukdom stadium 3 i själva verket har en relativt långsam minskning av GFR, särskilt om de har låg albuminutsöndring i urinen och välkontrollerat blodtryck. Därför kan den låga prevalensen av stadium 4 och 5 jämfört med stadium 3 bero på att en del äldre med stadium 3 inte har allvarlig njursjukdom utan en fysiologisk, åldersrelaterad långsam minskning av GFR. Upprepade mätningar av eGFR hos äldre, kompletterat med bedömning av andra riskfaktorer som albuminuri och blodtryck, kan troligen identifiera dem som har en snabbare progress av sin njursjukdom, som kan kräva ett mer selekterat medicinskt omhändertagande.
Konsekvenser av kronisk njursjukdom
Flera stora och välgjorda observations- och populationsstudier har visat att måttligt till kraftigt nedsatt njurfunktion är förenad med ökad risk för infektion, bensjukdom och kardiovaskulär morbiditet och mortalitet. Nyligen publicerade analyser av stora populationer visar att risken för mortalitet och kardiovaskulär sjukdom hos patienter med njursjukdom är i paritet med den vid diabetes eller hypertoni (11-13). Sannolikt föreligger ett direkt kausalt samband mellan sjunkande njurfunktion och ökad kardiovaskulär morbiditet, även om mekanismerna fortfarande är osäkra och omdiskuterade.
Om albuminuri adderas som riskfaktor till njursvikt förstärks sambandet än mer [14]. Sjunkande njurfunktion leder inte bara till vätskeretention med hypertoni och risk för hjärtsvikt, utan också till en rad rubbningar i benmineralmetabolismen, rubbad hemostas, renal anemi, kronisk låggradig inflammation och till hormonella störningar. Kardiorenala syndromet typ 4 sammanfattar de mekanismer som är involverade i utvecklingen av hjärt–kärlsjukdom sekundärt till kronisk njursjukdom liksom de kardiella konsekvenserna [15].
Data från Swedeheartregistret visar att patienter med hjärtinfarkt som också har njursjukdom har sämre prognos det första året efter insjuknandet, och att de inte får behandling enligt gängse riktlinjer [16]. Mycket forskning behövs under kommande år för att öka kunskapen om sambandet mellan njurfunktion och hjärtsjukdomar, och vice versa, samt för att förbättra behandlingen av personer med nedsatt njurfunktion och samtidig hjärt–kärlsjukdom.
Screening för förekomst av njursjukdom
I dag undersöks de flesta patienter med hypertoni och diabetes systematiskt för förekomst av albuminuri och andra tecken på njursjukdom, och den medicinska behandlingen med t ex ACE-hämmare anpassas därefter. I HUNT 2-studien hade 4,7 procent nedsatt eGFR mindre än 60 ml/min/1,73 m2 vilket innebär att man måste screena 21 personer för att identifiera en individ med kronisk njursjukdom.
En mer specifik screening av individer i befolkningen med hypertoni, diabetes eller ålder över 55 år skulle identifiera 93 procent av alla patienter med kronisk njursjukdom. Antalet individer som behöver screenas blir då nio [17]. Detta talar för att en screening med syftet att tidigt identifiera och behandla patienter med lätt till måttlig njursjukdom med t ex ACE-hämmare bör vara fokuserad på högriskpopulationer som patienter med diabetes, högt blodtryck, äldre individer och patienter med känd kardiovaskulär sjukdom. Frågan om allmän screening är dock mycket omdiskuterad.