Den ökande användningen av opioider för behandling av långvarig smärta har utvecklats till ett folkhälsoproblem i Sverige såväl som i andra länder.
Följderna är problematiskt bruk, beroende och en ökad dödlighet på grund av läckage till ungdomar och riskgrupper.
Ytterligare effekter av långtidsanvändning vid svåra sjukdomar är toleransutveckling och bristande effekt.
Situationen kan jämföras med överanvändning av antibiotika och därmed följande resistensutveckling.
Nya åtgärder och riktlinjer är påkallade för att bevara opioidernas smärtlindrande effekt, som att tidsbegränsa användningen och införa takdoser.
Former för samarbete och vårdkedjor bör upprättas för komplicerade fall.
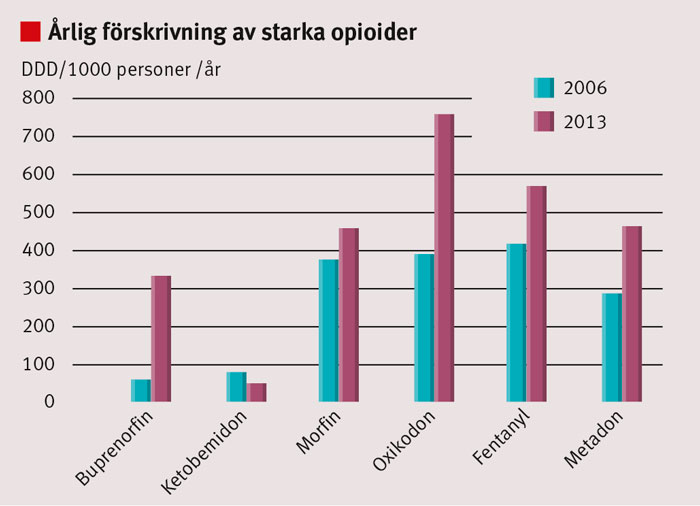
Figur 1. Förskrivning av opioider 2006 och 2013. DDD = definierade dygnsdoser. Källa: Socialstyrelsens läkemedelsstatistik för riket, båda könen i åldrarna 30–85+.
De morfinliknande läkemedlen, opioiderna, är fortfarande det bästa vi har att erbjuda vid akut smärta och cancer. För dessa tillstånd finns god klinisk erfarenhet gällande effektivitet och en fast grundad evidens. Däremot är situationen för användning av morfinläkemedel vid svår långvarig smärta kontroversiell, och evidensen för framgångsrik behandling saknas [1, 2]. Trots detta har förskrivningen av opioider ökat mångfaldigt i takt med att långvarig smärta uppmärksammas som ett folkhälsoproblem [3], se Figur 1. Studieresultat och metaanalyser gällande smärtlindring och förbättring av livskvalitet är motstridiga, och längre studier av god kvalitet lyser med sin frånvaro [4, 5].
Larmrapporter både från Sverige och USA vittnar om ökad dödlighet av legalt förskrivna opioider, framför allt metadon [3, 6]. Dödsfallen förekommer i missbrukskretsar, men också i andra grupper, vid suicid och oavsiktliga överdoseringar. Långtidsbiverkningar som hormonrubbningar, immunologisk påverkan och smärtöverkänslighet utlöst av själva opioiden (opioidhyperalgesi) begränsar ytterligare möjligheterna till ett gynnsamt behandlingsutfall. Tolerans, beroende och problematiskt bruk av opioider är andra faror på vägen, med kognitiv påverkan och sämre förutsättningar för hantering och rehabilitering [7]. Detta blir en belastning för patient, sjukvård och samhälle.
Toleransutveckling, allvarliga biverkningar och överhuvudtaget tveksam smärtlindrande effekt över tid är fenomen som kan leda tanken till situationen för antibiotika. Överanvändningen av antibiotika har lett till en resistensutveckling, där vi på sikt kan stå helt utan effektiva medel vid svåra infektioner. Är vi på samma väg med vår överförskrivning av opioider till allt fler grupper av smärtpatienter? Hur hjälper vi den svårt sjuke cancerpatienten som blivit opioidtolerant eller i värsta fall opioidresistent efter långvarig opioidbehandling av ett kroniskt smärtsyndrom?
Riktlinjer följs inte
Enligt riktlinjer som utstakades 2002 är användning av opioider för kronisk smärta en undantagsbehandling och en sista utväg till patienter med svåra smärttillstånd i paritet med en cancersjukdom. All annan behandling ska ha prövats, inkluderande kognitiv beteendeterapi och multidisciplinär handläggning. Patienten ska ha genomgått en smärtanalys, och opioidkänslighet ska fastställas. En riskbedömning ska vara utförd och beroendeaspekten uppmärksammas. Ett kontrakt kan upprättas med behandlingsmål som ska följas och utvärderas. Kontinuitet och uppföljning ska poängteras. Morfin är förstahandsmedlet, och långverkande beredningar ska användas. Injektionsbehandling ska undvikas.
I dag, drygt tio år senare är dessa principer fortfarande aktuella, men har inte använts kliniskt i den utsträckning som var avsikten. I stället ter sig den kliniska verkligheten alltmer komplex.
Fler överlever och lever med cancer
Ingen ifrågasätter i dag att cancersmärta kan och ska behandlas med opioider. Men situationen ser annorlunda ut i dag än för 10–20 år sedan. I dag är cancer en sjukdom som botas i mer än 50 procent av fallen. Många lever dessutom länge med en cancersjukdom eller med följderna av kirurgiska ingrepp, strålbehandling eller cytostatika. Därför kan en cancerpatient i icke terminalt skede i de flesta fall jämföras med en patient med svår icke-cancerrelaterad smärta, med samma risk för problematiskt bruk av opioider [8]. En del av cancerpatienterna har också psykiatriska tillstånd och beroendesjukdomar som väsentligt försvårar en välfungerande opioidbehandling.
Flera aktuella studier visar också att de som använder starka opioider under längre tid, och framför allt i höga doser, är patienter som utöver sitt smärttillstånd har svåra psykiatriska sjukdomar och smärtor från flera olika delar av kroppen [9, 10]. Andra riskfaktorer för högdos-opioidbehandling är hjärt–kärlsjukdomar, kronisk obstruktiv lungsjukdom, begåvningshandikapp, låg utbildning, kaotisk livsstil, tidigare beroendeproblem och en utsatt psykosocial situation [11].
Det finns grupper av patienter med multipla somatiska och psykiatriska sjukdomar som genomgår upprepade operationer med svår generaliserad smärta, komplicerad av psykiska, sociala och existentiella komponenter med ett lidande motsvarande det vid en terminal cancersjukdom [12]. Målet blir då inte bara att lindra den nociceptiva och opioid-responsiva smärtan, utan en mer palliativ behandling. Till skillnad från vid en svår cancersjukdom i terminalskede kan opioidbehandlingen dra ut på tiden, med risk för toleransutveckling och dosökning.
De flesta erfarna kliniker menar dock att det finns idealpatienter som svarar bra på låga doser opioider, återgår eller kvarstår i arbete och behåller samma dos år efter år med ett minimum av biverkningar. Individer i denna grupp utgör sällan problem och ska självklart inte heller missunnas behandling.
Provbehandling med aktuell peroral opioid och en systematisk uppföljning av grad av smärtlindring, effekt på funktion och livskvalitet är en bra metod. Emellertid kräver detta avsevärd tid för dostitrering och optimering mellan effekt och biverkningar. Den tiden finns knappast på allmänläkarmottagningen eller ens på smärtkliniken, bägge verksamheter med krav på att erbjuda god tillgänglighet och korta väntetider.
Olika typer av beroende och missbruk
Fysiskt beroende. Under liberaliseringen av opioidanvändningen vid slutet av 1980-talet påstods det att det inte fanns någon risk för beroende så länge patienten hade smärta. Tyvärr visade det sig snart att de flesta, inklusive cancerpatienter, som använde opioider utvecklade ett fysiskt beroende och fick abstinenssymtom vid abrupt behandlingsavbrott eller snabb dosminskning. Dessa fenomen är fysiologiska och gemensamma för många farmaka, inte bara opioider. Beroende- och missbruksdiagnoser enligt den amerikanska psykiatriklassifikationen DSM-IV(5) och den internationella sjukdomsklassifikationen ICD-10 kan vara svåra att tillämpa på smärtpatienter som får sina opioider förskrivna för medicinskt bruk. Därför har ytterligare terminologi föreslagits som komplettering, se nedan. I den nya diagnosmanualen DSM-5 är missbrukstermen dessutom borttagen. Missbruk hänför till illegal aktivitet, men används tyvärr ofta osakligt och har en stigmatiserande konnotation som inte befordrar en god patientrelation.
Problematiskt bruk och pseudoberoende. Ett problematiskt bruk är oauktoriserad dosökning, användning av flera förskrivare, borttappade och stulna recept och läkemedel samt frekventa besök på akutmottagning. Detta kan bero på en ofullständigt diagnostiserad och suboptimalt behandlad smärta, pseudoberoende, men kan också vara en förvarning om ett beroendeproblem eller kaotisk livsstil [13].
Psykiskt beroende. Ett psykiskt beroende är en neurobiologisk sjukdom med genetiska och sociala komponenter. Den yttrar sig i drogbegär, tvångmässighet, kontrollförlust och en ogynnsam beteendeförändring med psykosociala konsekvenser [14].
Iatrogent opioidberoende. Förskrivning av potenta kortverkande såväl som långverkande opioider och injektionsberedningar kan leda till ett iatrogent opioidberoende även hos patienter med primärt svår smärtproblematik.
Läckage av opioider förekommer också bland opioidbehandlade smärtpatienter. Man ger eller säljer till vänner och bekanta, men också på svarta marknaden. Motivet är att hjälpa en vän eller släkting i nöd eller att förbättra sin egen ekonomi. I dessa sammanhang finns många av de opioidrelaterade dödsfallen och ett växande samhällsproblem [15].
Riskfaktorer för problematisk opioidanvändning
I dag finns en etablerad kunskap om riskerna för problematisk opioidanvändning och beroende. Det är psykiatriska sjukdomar, psykosocial utsatthet och övergrepp, tidigare beroende och missbruk i anamnesen, samt förekomst av detsamma i familjen. Störst är risken vid pågående blandmissbruk. Ett problem som länge förblir dolt för sjukvårdspersonal är riskbruk och beroende av alkohol. Opioidbehandling kan ibland leda till alkoholsug och blandberoendet blir en stor hälsorisk med en avsevärd mortalitet [16]. Skamkänslor och ett starkt förnekande hos patient och medberoende familjemedlemmar gör att diagnosen ofta ställs allt för sent.
Psykiatriska diagnoser, särskilt ångestsyndrom, är också riskfaktorer för problem med opioidbehandling, där ångest och oro driver upp doserna. Risken för beroende föreligger även för de rekommenderade långverkande beredningarna. Det är opioiden i sig som är beroendeskapande.
Det förekommer sannolikt en underdiagnostik vad gäller alkoholproblem, begåvningshandikapp samt neuropsyki-atriska diagnoser bland smärtpatienter som svarar dåligt på behandling. I dessa fall är dessutom risken för iatrogena behandlingsskador stor. För alkoholriskbruk kan fosfatidyletanol (PEth) vara en användbar screeningmetod utöver anvisade formulär som AUDIT (Alcohol use disorders identification test).
Behandlingskontrakt används sällan
Användning av skriftliga behandlingskontrakt rekommenderas i Läkemedelsverkets riktlinjer [17], men används sällan. I dessa bör behandlingsmål och strukturerad uppföljning ingå. Kontinuiteten av förskrivande läkare är ett problem kopplat till bemanning och personalomsättning. En ansvarig förskrivare är inte alltid utsedd. Många patienter som behöver sin opioidbehandling står ibland utan förskrivare och riskerar abstinens och utebliven smärtbehandling. I andra fall skrivs opioider ut, ibland flera hundra tabletter åt gången, men med bristfällig uppföljning. Här finns uppenbara risker för både suboptimalt behandlad smärta och en okontrollerad opioidkonsumtion.
Morfin förstahandsmedel
Rekommendationen att använda morfin i första hand grundar sig på att medlet är väldokumenterat och billigt. Ingen god evidens finns för att någon opioid är bättre än någon annan på gruppnivå, men det finns stora individuella skillnader vad gäller effekt och biverkningar för olika opioider [18]. Förskrivningsstatistik visar dock att oxikodon och fentanyl förskrivs mer än morfin, se Figur 1 [19].
Morfin har många nackdelar, som aktiva metaboliter som ansamlas vid njurinsufficiens, hallucinationer hos känsliga individer, dålig och varierande peroral biotillgänglighet, samt en tendens till utveckling av hyperalgesi vid långtidsanvändning. Opioidhyperalgesi förekommer även med andra opioider och leder till en paradoxalt ökad smärta bland annat på grund av subcellulära förändringar i nervcellen. Till skillnad från vid toleransutveckling, som kan kompenseras med ökad dos, leder ökad dosering till ökad smärta vid opioidhyperalgesi [20]. Grundprincipen är att använda morfin i långverkande beredning i första hand och de andra starka opioiderna oxikodon, ketobemidon, fentanyl samt tapentadol som alternativ.
Buprenorfin är ett läkemedel med många verkningsmekanismer som börjar få en renässans som smärtläkemedel och kan utgöra ett ytterligare alternativ. Buprenorfin är en full agonist vad gäller analgesi med effekt på flera subtyper av opioidreceptorer och inverkan huvudsakligen på spinal nivå. Det innebär att risken för andningsdepression och neuroendokrina effekter är mindre än för de konventionella opioiderna [21].
Metadon används också ibland som ett billigt alternativ, bland annat i Danmark och USA. Sakligt skäl anges vara god effekt på svåra smärtttillstånd. Samtidigt är metadon preparatet med högst opioidrelaterad mortalitet. Det är svårstyrt med en stor variabilitet i farmakokinetik, många interaktionsrisker och risk för livshotande arytmier på grund av Q-T-förlängning [22]. Av dessa skäl bör metadon vara ett sista alternativ och endast förskrivas av smärtspecialister med god erfarenhet av metadonbehandling.
Vid behov av ökande dygnsdoser av opioider bör en gräns sättas för vidare dosökning. I de nyare riktlinjerna från Kanada och USA föreslås takdosen 120–180 mg morfinekvivalenter [23, 24]. Doser över denna gräns har inte visat sig ha gynnsam effekt vare sig för smärtlindring, funktion eller livskvalitet. I stället kan dosen sänkas med hjälp av opioidrotation, vilket innebär byte till annan opioid i lägre dos. Bakgrunden till detta är en inkomplett korstolerans mellan de olika opioiderna. Alternativet är att använda sig av adjuvans, i betydelse icke- opioida farmaka, som har egen analgetisk effekt, alternativt förstärker opioideffekten. Dessa läkemedel finns i grupperna antidepressiva och antiepileptika, men också kortikosteroider och klonidin kan användas.
Att långverkande beredningar är bäst för långtidsbruk har länge varit en »sanning«. Det visar sig dock i nya studier att patienter som kan ta kortverkande opioider vid behov utöver sitt långverkande medel har lägre dygnsdoser och mindre frekvens problematiskt opioidberoende [25]. Missbrukspotentialen för långverkande medel är inte försumbar, då dessa preparationer krossas och tas peroralt för snabbare effekt eller injiceras intravenöst alternativt inhaleras. Transdermala preparationer löses i vätska och dricks, injiceras eller antänds och inhaleras, ibland med dödligt utfall.
Trender och nyare riktlinjer
I dag diskuteras för och emot opioidbehandling vid kronisk smärta i debattartiklar och ledare i den medicinska litteraturen. Tongångarna är pessimistiska, även bland tidigare entusiaster [26]. Den liberala förskrivningen i USA och den stigande mortaliteten förknippad med legalt förskrivna opioider skrämmer. Myndigheter varslar om ny lagstiftning och hårdare kontroll. Få vill dock återgå till 1900-talets opiofobi och begränsade möjligheter att behandla svår smärta.
Den medicinska professionen försöker hitta nya evidensbaserade riktlinjer, och diskuterar krav på utbildning av förskrivare, dosbegränsning, dostak, riskbedömning samt hårdare kontroll av insatt behandling [23, 24]. Samtidigt diskuteras patientens behov och rättigheter till självbestämmande och individualiserad och skräddarsydd behandling. En avvägning mellan alla dessa hänsyn kräver en etisk och medicinsk balansgång.
Förslag på vårdnivåer
En allt vanligare patientgrupp i dagens sjukvård är de med ett aktuellt eller tidigare beroende som utvecklar svåra smärtsyndrom i samband med allvarliga sjukdomar, inte minst cancer, olycksfall och skador. De flesta av dessa patienter kräver ett multidisciplinärt och multiprofessionellt handläggande för att få en säker och fungerande behandling. En differentierad indelning kan göras av relevanta grupper för opioidbehandling:
1. Den klassiska opioidresponsiva patienten som uppnår god och stabil smärtlindring med en relativt låg dos utan annan problematik än sin smärta. Vederbörande kan sannolikt med fördel också genomgå smärtrehabilitering vid behov och skötas i primärvården.
2. Den komplicerade patienten med generell smärta, psykiatrisk och somatisk samsjuklighet och sociala komplikationer som kan bedömas utifrån ett palliativt synsätt och behandlas inom ramen för ett multiprofessionellt team. Här behövs ofta insats av sjuksköterska/koordinator/kurator för att samordna vårdinsatser. Konsultation av smärtpsykiater är önskvärt. Dessa patienter hör hemma på en smärtmottagning.
3. Patienter med problematiskt bruk av opioider i form av iatrogent injektions- eller högdosberoende med fortsatt svår smärtproblematik. Dessa patienter kan få fungerande opioidbehandling med metadon i liknande organisation och former som metadonprogrammen för heroinberoende. En del av patienterna kan även vara hjälpta av buprenorfin i dosering som ligger under de doser som används för heroinsubstitution. Buprenorfin är också ett gott alternativ för patienter som har alkoholanamnes eller andra kontraindikationer för metadonbehandling [27, 28].
4. Smärtpatienter med suicidrisk, pågående missbruk och psykoser. Dessa patienter får bäst omhändertagande inom psykiatrin och kan svårligen hanteras enbart på en smärtmottagning, men kan få förskrivning av opioid om samarbete finns mellan beroende- och smärtenheter. När man behandlar dessa patienter med allvarliga riskfaktorer bör man vara noga med struktur, dostak och skrivna behandlingskontrakt. Där behandling spårar ur och när det gäller patienter med blandmissbruk bör förskrivning och utdelning ske via beroendeklinik.
Gott samarbete krävs
Morfinläkemedlen, opioiderna, är goda läkemedel mot svår smärta som rätt använda kan ge många patienter lindring också vid långvarig smärta. Risker, biverkningar och komplikationer finns med alla läkemedel, också med opioiderna, som därtill behäftas med en risk för beroende. Från att ha använts mestadels vid akut smärta och cancer används opioiderna i dag huvudsakligen vid icke-cancerrelaterad smärta och på allt fler grupper av patienter med komplicerande sjukdomar och beroendeproblem. Eftertankens kranka blekhet drabbar oss när vi står inför den svårt sjuka och smärtplågade patienten som är opioidresistent. För att kunna fortsätta att erbjuda en god och relevant smärtlindring med opioider bör dessa användas enligt aktuell evidens och kunskap. Det gäller att tillämpa principen med takdoser och adjuvans, att begränsa användningen över tid och tillämpa yttersta restriktivitet när det rör sig om ungdomar och yngre vuxna. För att på ett trovärdigt sätt fortsätta denna process krävs noggrannhet i riskbedömning, uppföljning och framför allt ett gott samarbete mellan primärvård, smärt- och beroendekliniker. Det finns ett stort behov av att inrätta nya riktlinjer, fungerande vårdkedjor och kommunikation mellan olika specialiteter och vårdgivare.
Potentiella bindningar eller jävsförhållanden: Författaren har mottagit föreläsararvoden från GlaxoSmithKline och Grünenthal Sweden.






















