Tiopuriner används huvudsakligen för behandling av inflammatorisk tarmsjukdom och barnleukemi.
Tiopurinmetyltransferas (TPMT) är ett polymorft enzym som metaboliserar tiopuriner. Individer som saknar enzymet har ökad risk för utveckling av allvarliga biverkningar vid behandling med normala doser tiopuriner.
Bestämning av TPMT-status och tiopurinmetaboliter har betydelse för att dosanpassa och därigenom optimera användningen av tiopuriner, framför allt vid inflammatorisk tarmsjukdom.
Vid Linköpings universitet bedrivs forskning kring tiopurinfarmakogenetik. Sedan år 2000 har på klinisk indikation TPMT-status analyserats hos fler än 12 000 individer som ska påbörja tiopurinbehandling.
Ett välkänt problem vid läkemedelsbehandling är att olika patienter kan svara väldigt olika på samma läkemedel i samma dos. Många faktorer kan bidra till detta, till exempel skillnader i njurfunktion, andra samtidiga sjukdomar eller interaktion med andra läkemedel. Det har blivit allt tydligare att ärftliga faktorer kan spela en viktig roll för individuella variationer i farmakokinetik. Den vanligaste orsaken är en variation i DNA-sekvensen i gener för läkemedelsmetaboliserande enzymer där en enstaka nukleotid skiljer mellan olika individer, enbaspolymorfier (SNP). Sådana skillnader i enstaka nukleotider kan leda till aminosyrautbyten i det bildade proteinet och kan innebära att man får ett mindre aktivt eller helt inaktivt enzym. Detta leder då till en minskad eliminering av läkemedlet med ökad risk för biverkningar. I andra fall, när metaboliten står för effekten, till exempel vid behandling med kodein, kan ett inaktivt enzym (i det fallet enzymet CYP2D6) i stället leda till minskad läkemedelseffekt.
Stora förhoppningar om skräddarsydd och individualiserad läkemedelsbehandling har knutits till den snabba utvecklingen av molekylärbiologiska metoder. I dag kan man sekvensera hela genomet för under 8 000 kronor. Vi har emellertid lärt oss att kännedom om DNA-sekvensen inte ger fullständig information om proteinernas funktion. Regleringen av geners funktion är ännu delvis höljd i dunkel. Klart är dock att pretranskriptionella och posttranslationella variationer är av betydelse, till exempel metylering av DNA, och ökat intresse knyts därför till epigenetiken. Många läkemedel metaboliseras via olika vägar, och nedsatt metabolism i en väg kan kompenseras genom ökad metabolism i en alternativ väg. Detta har medfört att ökade kunskaper om genetiska variationer i cytokrom P450-enzymerna har haft begränsad klinisk nytta, eftersom många läkemedel som metaboliseras av ett cytokrom P450-enzym också har en alternativ metabol väg via ett annat enzym i gruppen. I vissa fall kan dock genotypning av dessa enzymer besvara kliniska frågor kring dålig effekt/toxicitet av läkemedel, till exempel vid behandling med neuroleptika, antidepressiva, antikoagulantia med flera. Dock har detta i dag inte implementerats som rutin i den kliniska vardagen.
Som ett led i att överbrygga gapet mellan forskning och klinik har det internationella forskningskonsortiet PharmGKB (www.pharmGKB.org) gett ut riktlinjer för hur farmakogenetiska data kan översättas till doseringsanvisningar för vissa läkemedel [1].
Tiopuriner
Tiopuriner (6-merkaptopurin, azatioprin och tioguanin) är gamla läkemedel utvecklade av nobelpristagaren Gertrude Elion på 1950- och 60-talen. De hade till en början stor betydelse för att bland annat kunna genomföra organtransplantationer, och har i dag stor användning framför allt vid inflammatorisk tarmsjukdom och som underhållsbehandling vid barnleukemi. En tidig erfarenhet var att vissa individer fick svåra biverkningar även vid normala doser. Medlen genomgår en mycket komplicerad metabolism där man anser att fosforylering till tioguaninnukleotider (TGN) är av störst betydelse för effekten. En alternativ metabol väg är metylering genom enzymet tiopurinmetyltransferas (TPMT), som dels genererar inaktiva metaboliter (meMP, meTG), men som också metylerar tioinosinmonofosfat (TIMP) till meTIMP, en potent inhibitor av de novo-purinsyntesen i cellen.
1980 visade Weinshilboum och medarbetare att TPMT är ett polymorft enzym och att 10–15 procent av den västerländska befolkningen har en aktiv och en inaktiv allel och därmed ett mindre aktivt enzym [2], Figur 1. En halv procent har två inaktiva alleler vilket leder till total avsaknad av enzymaktivitet, varvid metabolismen av tiopuriner styrs om till ökad fosforylering med svåra biverkningar vid behandling med normala doser. Denna kunskap har lett till att till exempel den amerikanska läkemedelsmyndigheten Food and Drug Administration (FDA) och British Society of Gastroenterology (BSG) rekommenderar att patienter ska feno- eller genotypas för TPMT innan behandling med tiopurin sätts in. Därigenom kan doseringen individualiseras redan från början. Oklarhet råder om det fysiologiska substratet för TPMT, och individer med defekt enzym avviker inte från dem med normalt enzym, det vill säga man har inte kunnat fastställa en fysiologiskt viktig roll för TPMT.
Databas för att studera tiopurinernas farmakologi
Vår forskningsgrupp vid avdelningen för läkemedelsforskning vid Linköpings universitet har under lång tid studerat tiopurinernas farmakologi. Det är unikt att så gamla läkemedel behåller sin plats i terapin. Eftersom de är kommersiellt ointressanta finns inga industrisponsrade studier, även om frågeställningar inte saknas. Azatioprin introducerades som en prekursor till merkaptopurin när tidiga farmakokinetiska studier på 1960-talet visade att merkaptopurin hade en mycket kort halveringstid. En obesvarad fråga är: finns det skillnader i effekter mellan läkemedlen? I Sverige används azatioprin främst som immunsuppressivt medel vid inflammatorisk tarmsjukdom (IBD) och merkaptopurin vid akut lymfatisk leukemi hos barn.
Vårt intresse var till en början fokuserat på onkologiska frågeställningar, till exempel vilken roll metaboliterna spelar för de kliniska effekterna. Så småningom etablerades ett nära samarbete med gastroenterologer, och vi började få blodprov från många centra i landet för feno- och genotypning av TPMT inför behandlingsstart och för bestämning av fosforylerade och metylerade metaboliter under behandling avseende råd om dosering. Vi har tagit oss an ett flertal vetenskapliga frågeställningar, uppkomna ur såväl kliniska som grundvetenskapliga problem. Under lång tid har vi också analyserat TPMT-aktiviteten hos barn med akut lymfatisk leukemi som får underhållsbehandling med 6-merkaptopurin under cirka 2 år. Barnen behandlas enligt ett nordiskt behandlingsprotokoll i vilket doseringen av 6-merkaptopurin är individualiserad med ledning av TPMT-genotypen.
I vår databas finns data från mer än 27 000 prov från cirka 16 000 individer. Mer än hälften av proven kommer från gastroenterologiska kliniker. Vanligaste diagnoser är Crohns sjukdom och ulcerös kolit. Många prov kommer också från patienter med reumatoid artrit. Cirka 5 procent av proven kommer från hematologiska kliniker. En mindre del kommer från dermatologiska kliniker och från transplantionsenheter.
TPMT-genotypning och -fenotypning
Från början utfördes enbart TPMT-aktivitetsbestämning på laboratoriet, men sedan 2006 bestäms alltid TPMT-genotyp och enzymaktivitet tillsammans. TPMT-enzymaktiviteten bestäms i röda blodkroppar med ett radioaktivt substrat, utvecklad av Weinshilboum et al [3]. Figur 1 visar den trimodala distributionen av TPMT-enzymaktivitet som återfinns i den svenska befolkningen [4].
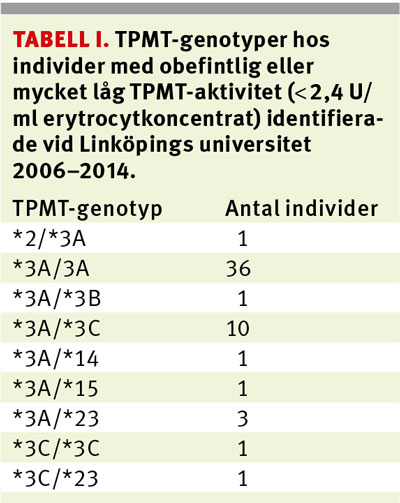
Genotypning med pyrosekvensering sker för de tre i västerländsk befolkning vanligaste sekvensvarianterna [5, 6]. I vår databas är 90 procent genotypade till homozygot normalvariant (*1/*1), det vill säga vildtyp, 9,5 procent bär på en icke-funktionell variantallel och 0,5 procent bär på två icke-funktionella alleler vilket stämmer väl överens med publicerade data från andra populationer. Totalt har vi identifierat 55 individer med total avsaknad av TPMT, Tabell I.
Nedan följer två exempel på konsekvenserna när patienter utan TPMT-aktivitet behandlas med vanliga doser av azatioprin.
Fall 1
Det första fallet rör en 83-årig man som under några år haft diffusa tarmbesvär. Mannen fick diagnosen obestämbar kolit (IBD-U) och behandlades med steroider efter ett skov med blodiga diarréer 6–8 ggr/dag. Man påbörjade behandling med azatioprin i steroidsparande syfte till en början 50 mg × 2 och sedan i reducerad dos på grund av sjunkande leukocyttal och trombocyter. Prov skickades för bestämning av TPMT och tiopurinmetaboliter, men patienten avled i en Aspergilluspneumoni innan svaret kommit, som visade att patienten helt saknade TPMT-aktivitet och hade skyhöga koncentrationer av de fosforylerade metaboliterna (TGN > 2 000 pmol/8 × 108 erytrocyter).
Fall 2
Ett annat fall med inte lika ödesdiger utgång gäller en 20-årig man med diagnosen granulomatös polyangit. Patienten, som vägde 82,5 kg, sattes in på azatioprin 100 mg × 2 och fick en pancytopeni. TPMT-analys visade att mannen var totaldefekt och hade skyhöga fosforylerade metaboliter, varför azatioprinet sattes ut. Patienten följdes sedan med upprepad provtagning, och det tog över en månad innan metabolitkoncentrationen var under den övre rekommenderade TGN-metabolitnivån (400 pmol/8 × 108 erytrocyter). Mannen återhämtade sig så småningom från sin pancytopeni.
De två fallen betonar betydelsen av att bestämma patientens TPMT-status före start av tiopurinbehandling.
Genotypning eller fenotypning – vad är att föredra?
Fenotypning (bestämning av enzymaktiviteten) ger ett funktionellt mått. Dock sker mätningen i de flesta laboratorier på tvättade röda blodkroppar, och det är osäkert i vilken mån detta avspeglar aktiviteten i målcellerna, det vill säga de vita blodkropparna i till exempel tarmslemhinnan. Det är väl känt att andra läkemedel kan påverka TPMT-aktiviteten, men detta återspeglas inte i laboratorieanalyserna eftersom de andra läkemedlen tvättats bort. Till exempel är det känt att olsalazin, mesalazin och sulfalazin kan öka risken för benmärgshämning [7], och studier på rekombinant TPMT-enzym har visat att dessa läkemedel binder till TPMT-proteinet [7-9]. Våra in vitro- och in vivo-studier visar att metotrexat binder till TPMT och hämmar aktiviteten av enzymet [10].
Ett annat problem vid fenotypning är patienter som erhållit blodtransfusion veckorna före provtagning. Barn med leukemi och störd erytropoes utgör ytterligare ett problem. Det är visat att åldrande röda blodkroppar har lägre TPMT-aktivitet än nybildade röda blodkroppar [11]. Därför bör genotypning snarare än fenotypning utföras då prov tas före det att patienten är i remission. I vårt material har 40 procent av barnen med leukemi en falskt låg TPMT-aktivitet, vilken sedan ökar i takt med att den egna blodkroppsproduktionen av röda blodkroppar återkommer. TPMT-aktiviteten vid remission överensstämmer väl med genotypen [10].
TPMT-diskrepanser
Hos 45 st (0,4 procent) av de individer som vi bestämt -TPMT-aktiviteten på föreligger intermediär eller mycket låg TPMT-aktivitet, men genotypning för de tre vanliga sekvensvarianterna har inte kunnat förklara den låga enzymaktiviteten. Som enda laboratorium i Sverige utför vi då rutinmässigt sekvensering av alla kodande delar av TPMT-genen, och hos 13 av de 45 patienterna har vi hittat ovanliga eller tidigare okända TPMT-sekvensvarianter som förklarat sänkt TPMT–aktivitet. I vår tvärvetenskapliga forskargrupp har vi då gått vidare och studerat effekten av de nya varianterna på aktiviteten av enzymet. Vi har även genom familjestudier kunna konfirmera att de nya varianterna ärvts från en av föräldrarna [6, 12, 13]. Hos övriga 22 individer har vi inte, trots sekvensering av de kodande delarna av TPMT-genen, kunnat hitta någon förklaring till den låga aktiviteten.
Hos en del TPMT-heterozygota individer med en variant TPMT-allel finner vi i stället en oförväntat hög aktivitet. Olika förklaringar kan finnas, till exempel har det visats att metylgruppsdonatorn S-adenosylmetionin stabiliserar TPMT-proteinet, vilket är mer uttalat hos TPMT-heterozygota individer [14, 15], och här skulle genetiska variationer i andra enzymer som påverkar stabiliteten av TPMT-proteinet kunna vara av betydelse liksom epigenetiska mekanismer såsom DNA-metylering. Tillsammans med europeiska och amerikanska forskare försöker vi nu klargöra dessa variationer i aktivitet.
Ett exempel kommer från en familj där vi identifierat en ny TPMT-polymorfi, en SNP i startkodonet av TPMT-proteinet, Figur 2. Initialt analyserades TPMT-aktiviteten hos en flicka med IBD. Aktiviteten var mycket låg och torde vara resultatet av två inaktiva TPMT-alleler. Vid genotypning för de tre vanligaste polymorfierna fann vi dock endast en icke-funktionell allel (*3A). Senare sekvensering av alla kodande delar av TPMT-genen visade att patienten även hade ett basutbyte i själva startkodonet av TPMT-mRNA, vilket orsakade ett defekt TPMT-protein. Prov från föräldrarna visade att den nyupptäckta polymorfin nedärvts från pappan, medan den tidigare kända allelen (*3A) nedärvts från mamman. I överensstämmelse med genotypen hade båda föräldrarna intermediär TPMT-aktivitet. Allelen innehållande den nya SNPen namngavs till TPMT*14 [6].
TPMT-nomenklatur
I takt med att det blivit lättare och går snabbare att sekvensera DNA rapporteras nya polymorfier i TPMT-genen, hittills 40 stycken. TPMT har sedan de första varianterna av genen publicerades namngivits med allelnomenklatur i likhet med flera andra läkemedelsmetaboliserande enzymer (t ex CYP450-enzymerna). Vid publicering av en ny TPMT-polymorfi har författarna namngivit allelen utifrån den allelinformation som de hittat i publicerade artiklar. Detta tillvägagångssätt har resulterat i att flera alleler har fått samma nomenklatur, fast de innehåller olika polymorfier.
Det var mot bakgrund av detta som M Appell tog initiativet till och startade TPMT-nomenklaturkommittén i samarbete med andra forskare utanför Sverige. Syftet med TPMT-nomenklaturkommittén är att ansvara för namngivning av nya TPMT-alleler [16]. De alleler som i olika publikationer definierats innehålla olika polymorfier fick nya allelbeteckningar. En hemsida fungerar som plattform för kommitténs arbete, där det via ett formulär enkelt går att anmäla en ny SNP (www.imh.liu.se/tpmtalleles). Kommittén värderar om det finns tillräckliga data för att visa att polymorfin leder till en funktionell förändring av TPMT-enzymet, och tillhandahåller i sådana fall ett allelnummer före publikation.
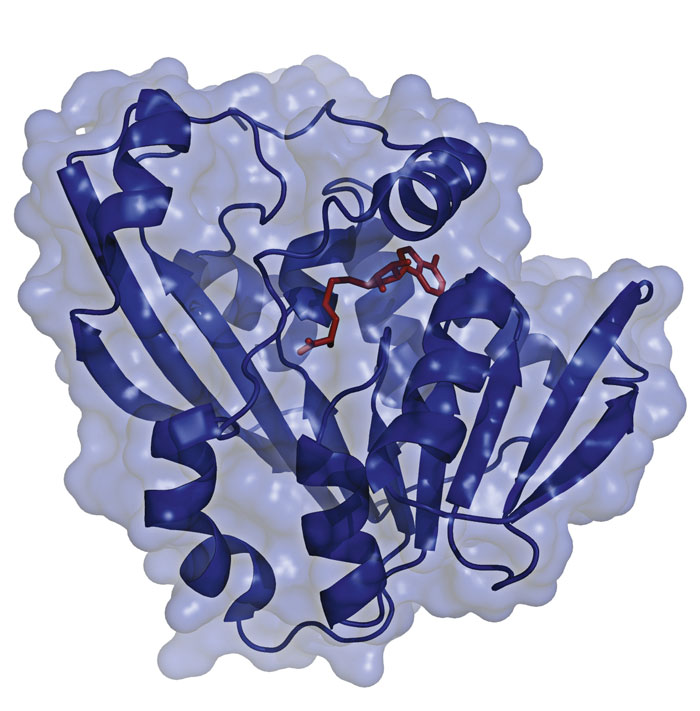
Strukturbiologiska studier av TPMT
Den tredimensionella strukturen av humant TPMT (Figur 3) bestämdes 2007 och har möjliggjort mer detaljerade studier på molekylär nivå. Vid tekniska fakulteten på Linköpings universitet har vi med hjälp av E colibakterier tillverkat ett flertal humana TPMT-proteinvarianter. Gemensamt för många av dessa TPMT-varianter är deras låga enzymaktivitet. Vad är orsaken till den låga enzymaktiviteten dessa varianter uppvisar?
Ett exempel är varianten TPMT*31 (tidigare namngiven till TPMT*28) [13] där vi kunde visa att den låga aktiviteten inte beror på aminosyrabyten i sig utan att den har lägre stabilitet och därmed bryts ned snabbare [13, 16]. Vi har nu utökat vår repertoar till att studera bindning med hjälp av olika biofysikaliska mätmetoder för att få en ingående förståelse hur olika läkemedel kan interagera med TPMT [10].
Andra gener av betydelse för tiopuriners effekt
Vid sidan av TPMT-enzymet och dess roll för att förutsäga toxicitet vid tiopurinbehandling, lyfts nu flera andra kandidatgener fram för att ytterligare förklara individers olika svar på tiopurinbehandling. Till exempel har polymorfier i genen för ABCC4 (ett transportprotein) [17-19] samt i ITPA-genen [20-22] associerats med biverkningar under tiopurinbehandling av leukemi. Andra leukemistudier har hittat samband mellan ITPA-polymorfi och överlevnad [23]. Det verkar som om effekten av ITPA-polymorfi på uppkomst av biverkningar blir tydlig först när dosering av 6-merkaptopurin justerats utifrån TPMT-aktivitet.
ITPA-genen kodar för det humana proteinet ITPas, och studier har visat att olika alleler av ITPA-genen kan minska ITPas-aktiviteten [24]. ITPas roll i cellen är att skydda cellen mot ackumulering av ITP, vilket i stora mängder inkorporeras i DNA. ITPas är involverat i metabolismen av tiopuriner. Defekter i genen för ITPas och TPMT leder vid tiopurinbehandling till ackumulering av TITP och metyl-TITP och troligen ökad inkorporering av TGN i DNA och RNA [25].
Resultaten från studier på patienter med IBD är mindre tydliga än vid leukemi. Sedan 2004 har det publicerats flera prospektiva och retrospektiva studier som påvisar ett samband mellan ITPA-polymorfi och biverkningar [26-29], men lika många som inte hittar dessa samband [30-33].
Mätning av tiopurinmetaboliter
Vid laboratoriet i Linköping mäts, förutom TPMT, också tiopurinmetaboliter i form av TGN och metylerade metaboliter (meTIMP) i helblod. Enligt en tidigare studie är refraktär sjukdom det främsta skälet till att mäta metabolitkoncentrationer vid IBD [34]. Andra anledningar till att beställa metabolitkoncentrationsmätningar är fråga om ordinationsföljsamhet eller som underlag för dosjustering om otillräcklig effekt eller vid biverkningsuppkomst som misstänks orsakas av tiopurinbehandling. Detta görs främst hos patienter med IBD och har blivit ett viktigt instrument för att optimera behandlingen av dessa kroniska inflammationssjukdomar.
Avvikande eller så kallad skev metabolism
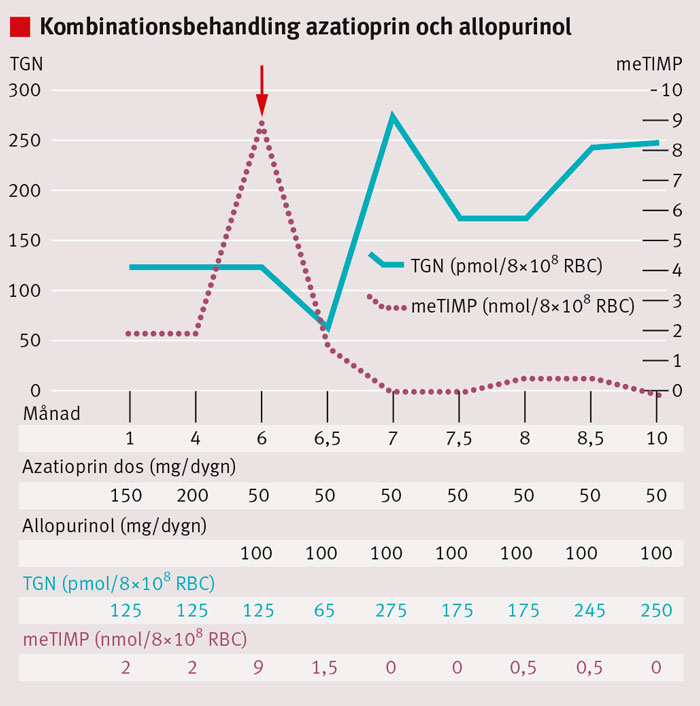
En så kallad skev tiopurinmetabolism ses hos upp till var femte patient med IBD och är förenad med bristande effekt och risk att drabbas av biverkningar [35-38]. Vid skev metabolism uppmäts låga TGN-nivåer i kombination med höga nivåer meTIMP. Kombinationsbehandling med lågdos tiopurin (25–30 procent av normaldos) och lågdos allopurinol (»ThioComp«) korrigerar den skeva metabolismen (Figur 4), vilket leder till ökad tolerans och bättre effekt. Oförmåga att producera adekvata TGN-nivåer är förknippad med dålig effekt av tiopurinbehandling [39, 40], och ovanligt höga koncentrationer metylerade metaboliter har satts i samband med såväl myelotoxicitet [32] som leverpåverkan [39]. Dessa patienter har ökad risk för såväl dåligt behandlingssvar som biverkningar. Patienter med skev metabolism har en normal TPMT-aktivitet medan detta metabolitmönster inte ses hos patienter med nedsatt TPMT-aktivitet.
Utifrån tidigare klinisk erfarenhet har kombinationsbehandling med tiopurin och allopurinol ansetts vara absolut kontraindicerad på grund av biverkningsriskerna. Såväl våra egna data [41] som data från andra centra [40] talar dock för att denna behandlingsstrategi är framgångsrik utan betydande ökad risk för uppkomst av biverkningar jämfört med monoterapi. De flesta patienter som haft leverpåverkan vid standardbehandling med tiopuriner tolererar kombinationsbehandlingen väl utan att återfå levertoxicitet. Omvänt kan det finnas patienter som uppvisar nytillkommen leverpåverkan under kombinationsbehandlingen, men denna är i så fall ofta lindrig [37]. Tillgång till bestämning av tiopurinmetaboliter är helt avgörande för att nå en effektiv behandling eftersom läkemedelsdosen kan justeras såväl uppåt som nedåt beroende på TGN-bestämningarna.
Barn med leukemi som behandlas med tiopurin och har sänkt TPMT-aktivitet (heterozygoter) har lägre nivåer av de hepatotoxiska metylerade metaboliterna och högre nivåer av de fosforylerade, samt lägre risk för återfall. I en fallrapport rörande en flicka med akut lymfatisk leukemi beskrivs ett framgångsrikt tillägg av tioguanin till den traditionsenliga underhållsbehandlingen innehållande 6-merkaptopurin och metotrexat, vilket hos patienten resulterade i att den skeva metabolismen korrigerades till mer fosforylerade metaboliter och mindre metylerade, likt den bild man ser hos heterozygota patienter [42], vilka har en mindre risk för återfall. En nu pågående nordisk-baltisk studie rekryterar patienter för att studera detta vidare.
Tiopuriner i framtiden
Även om nyare läkemedel för behandling av till exempel inflammatoriska sjukdomar introducerats (t ex TNF-hämmare), fortsätter tiopurinerna att vara ett betydelsefullt alternativ som kortisonsparande läkemedel. 6-merkaptopurin har sedan länge varit en hörnsten i underhållsbehandlingen av akut lymfatisk leukemi hos barn, både i Europa och USA. Nyligen publicerade studier lyfter fram nya potentiella markörer kopplade till behandling med bland annat tiopuriner vid barnleukemi [43, 44].
I vår forskargrupp studerar vi nu nya genetiska markörer som kan bli aktuella för farmakogenetisk typning före tiopurinbehandling. Vår och andras forskning försöker således hitta nya möjligheter att individualisera tiopurinbehandling [45]. I dag är bestämning av TPMT och tiopurinmetaboliter ett av relativt få lyckosamma farmakogenetiska bidrag till en förbättrad läkemedelsbehandling.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.




![Figur 1. Frekvensdistribution av TPMT-aktivitet i en svensk befolkning. Bilden visar kopplingen mellan funktionella och icke-funktionella anlag av TPMT-genen och dess resulterande TPMT-aktivitet. Figuren visar också dosrekommendationer utifrån TPMT-status enligt det nordiska protokollet för behandling av barn med akut lymfatisk leukemi. Figuren är modifierad från [4]. pRBC = erytrocytkoncentrat. NOPHO = Nordisk förening för pediatrisk hematologi och onkologi.](https://lakartidningen.se/wp-content/uploads/EditorialFiles/7L/%5bDF7L%5d/farmakogenetik_01_webb.jpg)
![Figur 2. Släktträd över den familj där den nya allelen TPMT*14 identifierades [10]. (pRBC = erytrocytkoncentrat)](https://lakartidningen.se/wp-content/uploads/EditorialFiles/7L/%5bDF7L%5d/farmakogenetik_02_webb.jpg)