Patienter med cirros har en ökad risk att ådra sig infektioner och en försämrad förmåga att spontanläka dessa.
Patienter med cirros kan betraktas som immunbristpatienter. Vid cirros bör man vara frikostig med odling från blod, urin, luftvägar och eventuella misstänkta fokala infektionsfokus samt tidig empirisk antibiotikabehandling vid plötslig försämring, även i frånvaro av CRP- eller prokalcitoninstegring.
De vanligaste infektionerna är spontan bakteriell peritonit, UVI och pneumoni.
Korrekt diagnostik och tidigt insatt behandling är av stor vikt för att minska dödligheten.
Patienter med varixblödning ska erhålla omedelbar antibiotikaprofylax. Antibiotikaprofylax efter en episod med spontan bakteriell peritonit kan vara indicerad vid avancerad cirros.
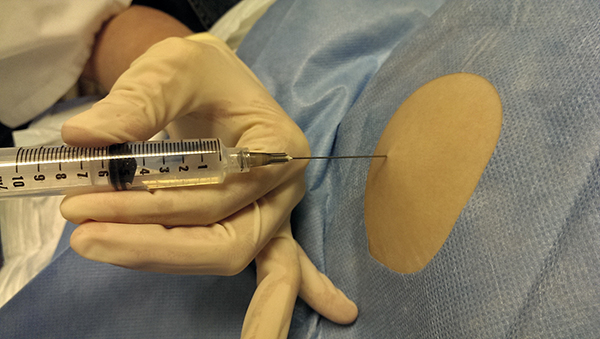
Figur 1. Diagnostisk buktappning.
En av de vanligaste dödsorsakerna hos patienter med cirros är infektioner. Så många som 32–34 procent av sjukhusvårdade patienter med cirros har eller utvecklar en infektion under vårdtiden, vilket kan jämföras mot 5–7 procent hos sjukhusvårdade patienter generellt [1, 2]. Patienter med cirros har också en ökad risk att dö av infektioner jämfört med patienter utan cirros. De vanligaste infektionerna hos patienter med cirros är spontan bakteriell peritonit (25 procent), urinvägsinfektion (20 procent) och pneumoni (15 procent). Diagnostiken försvåras av att infektioner hos patienter med cirros inte alltid ger upphov till CRP- och prokalcitoninnivåer som ses vid infektioner hos patienter utan cirros. En infektion är ofta det som initierar en snabb försämring av leverfunktionen, så kallad akut-på-kronisk leversvikt (se separat artikel i temat).
Patofysiologi
Patienter med cirros har ett sämre fungerande immunförsvar [3], beroende på flera faktorer som involverar både det humorala och det adaptiva immunsystemet. Bland annat har dessa patienter en nedsatt neutrofilfunktion och låga nivåer av komplement, vilket medför en försämrad förmåga att döda främmande organismer. Cirros leder också till nedsatt tarmmotorik och ofta till bakteriell överväxt i tunntarmen [4]. Tarmbakterier, framför allt gramnegativa såsom E coli, kan vid cirros translokera från tarmen till mesenteriska lymfknutor och spridas vidare i kroppen med risk för spontan bakteriell peritonit vid manifest ascites. Anaeroba infektioner är däremot ovanliga. Många patienter med cirros är undernärda och/eller medicinerar dessutom ibland med immunmodulerande läkemedel såsom kortison, vilket ytterligare ökar risken för infektion. Vidare leder portosystemisk shuntning via kollateraler, till exempel esofagusvaricer, blodflödet förbi levern, vilket innebär att patogener från tarmen undgår immunsystemet i levern med risk för bakteremi/sepsis. Sammantaget innebär ovanstående att patienter med cirros är en grupp med risk för att få infektioner och nedsatt förmåga att eliminera dessa.
Spontan bakteriell peritonit. Spontan bakteriell peritonit representerar den vanligaste infektionen hos patienter med cirros [5]. Dödligheten är hög, ca 20–30 procent, trots insatt behandling. Infektionen ger ingen lokal peritonitretning utan symtomen är ofta diffusa och inkluderar generell buksmärta, feber, illamående, takykardi, kräkning och ileus. Spontan bakteriell peritonit och andra infektioner utlöser ofta en försämring av leverfunktionen med risk för bland annat varixblödning, njurfunktionsnedsättning och encefalopati. SIRS (systemiskt inflammatoriskt svarssyndrom), sepsis, multiorgansvikt och död är vanligt vid obehandlad spontan bakteriell peritonit. Att korrekt identifiera och tidigt behandla ett sådant tillstånd är alltså centralt. Det är dock viktigt att poängtera att spontan bakteriell peritonit också kan vara asymomatisk, åtminstone initialt.
Alla patienter med känd eller misstänkt cirros och ascites som kommer till akutmottagning eller annan vårdinrättning med försämrad leverfunktion eller misstänkt spontan bakteriell peritonit bör genomgå diagnostisk buktappning (Figur 1). Denna bör normalt ske i vänster fossa motsvarande McBurneys punkt, där risken för stickblödning är som minst. Efter steriltvätt och med eller utan lokalanestesi kan en vanlig intramuskulär nål användas för att punktera buken, varefter man aspirerar 10–20 ml ascitesvätska. Denna är i normala fall klar och halmgul; vid grumlig ascites kan spontan bakteriell peritonit misstänkas. Diagnostisk buktappning kan ersättas av terapeutisk buktappning vid spänd, symtomgivande ascites.
Ascitesvätskan analyseras för leukocyter. Ett rör sparas i kyl för odling vid positivt fynd, som utgörs av polynukleära neutrofiler > 0,25 × 103/ml eller > 0,5 × 103/ml totala leukocyter som dock har lägre specificitet. Diagnosen spontan bakteriell peritonit kan då ställas, om inte annan rimlig förklaring finns såsom bukabscess eller blödning. Blododling görs samtidigt.
Vid positivt fynd för leukocyter i ascites ska behandling sättas in utan att odlingssvar inväntas. Behandling utgörs lämpligen av tredje generationens cefalosporinpreparat, till exempel cefotaxim 1 g × 3, som täcker de vanligaste gramnegativa patogenerna. Vid positivt odlingssvar specificeras behandlingen mot orsakande patogen. I 60 procent av fallen av spontan bakteriell peritonit är odlingen negativ; dock ska behandling i dessa fall fortsätta. Behandlingstid är i normalfallet fem dagar, varefter övergång till profylaktisk behandling enligt nedan bör övervägas.
Tillägg av albumin till cefotaximbehandling vid spontan bakteriell peritonit har i en randomiserad kontrollerad studie visat sig sänka mortaliteten från 29 till 10 procent. Mortalitetsminskningen var störst hos patienter med bilirubin > 40 µmol/l eller kreatinin > 88 µmol/l. Framför allt verkar risken för att utveckla njurfunktionsnedsättning och hepatorenalt syndrom typ 1 minska [6]. Patienter med verifierad spontan bakteriell peritonit bör därför erhålla albumin i dosen 1,5 g per kilo vid diagnos och 1 g per kilo två dagar senare [5]. När det gäller andra infektioner än spontan bakteriell peritonit visade en nyligen publicerad randomiserad kontrollerad studie ingen säker överlevnadsvinst hos albuminbehandlade patienter [7], varför detta i nuläget inte kan rekommenderas generellt.
En del patienter med ascites utvecklar, på grund av mikroperforationer i levernära diafragma, också högersidig pleuravätska. Denna kan också bli infekterad och behandling sker då på samma sätt som vid spontan bakteriell peritonit.
Profylax och vidare handläggning. Risken att inom 1 år utveckla en ny episod med spontan bakteriell peritonit är 70 procent. Denna risk kan minskas till ca 20 procent om patienten erhåller profylax med antibiotika [8]. Traditionellt rekommenderas profylax tills ascitesvätskan försvunnit eller tills patienten genomgått levertransplantation [9]. En individuell anpassning ska dock alltid göras. I nuläget finns bäst evidens för att använda norfloxacin [8, 10], men på grund av hög risk för resistensutveckling används i Sverige primärt ciprofloxacin i dosen 500 mg × 1.
Andra infektioner
Övriga infektioner såsom UVI, pneumoni och hudinfektioner är också vanliga. Dödligheten hos patienter med cirros är även vid dessa, annars ofta banala, infektioner hög. Man bör vara mycket liberal med odling (inklusive svampodling) från blod, urin, luftvägar samt eventuella misstänkta fokala infektionsfokus och empirisk behandling med bredspektrumantibiotika. Ofta har infektionerna utgått från sjukvårdsrelaterade infartsportar såsom KAD eller PVK. I en nyligen publicerad svensk studie var två tredjedelar av infektioner hos patienter med cirros sjukvårdsrelaterade [11]. Identifiering av infektionsfokus är viktigt, och vårdpersonal bör vara mycket noggrann gällande basala hygienrutiner.
Antibiotika vid varixblödning
Varixblödning är en fruktad komplikation till cirros. Många av dessa patienter har antingen en manifest infektion, som troligen bidragit till blödningen, eller utvecklar en infektion under vårdtiden. Tidigt insatt profylax med bredspektrumantibiotika har visat sig minska mortaliteten med minst 10 procent [12]. Alla patienter med cirros som inkommer till sjukvården med övre gastrointestinal blödning bör i tillägg till övrig behandling omedelbart erhålla intravenösa bredspektrumantibiotika, förslagsvis cefotaxim 1 g × 3 i 7 dagar [5] (se även separat artikel i temat).
Övriga synpunkter
Protonpumpshämmare har misstänkts vara en riskfaktor för infektioner hos patienter med cirros. I en nyligen publicerad amerikansk studie ökade behandling med protonpumpshämmare risken för infektioner med nästan tre gånger hos cirrospatienter [10]. Förskrivning av protonpumpshämmare till patienter med cirros ska göras på strikta evidensbaserade grunder och inte slentrianmässigt på grund av oklar buksmärta.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
























