Det finns två huvudtyper av inhalatorer: pulverinhalatorer (DPI, dry powder inhalers) och inhalatorer som producerar aerosol (pMDI, pressured metered dose inhalers samt SMI, soft mist inhalers).
Handhavande och inhalationsteknik skiljer sig avsevärt mellan olika inhalatortyper. Olika inhalatorer passar olika patienter.
Många patienter har felaktigt handhavande/felaktig inhalationsteknik.
Val av inhalator har stor betydelse för behandlingsresultatet.
Kombination av olika inhalatortyper ökar risk för handhavandefel.
Noggrann instruktion och uppföljning av inhalationsteknik är viktigt för alla patienter vid varje besök, ofta via astma/KOL-sjuksköterska.
Byte av inhalator bör övervägas vid behandlingssvikt.
Byte av inhalator utan instruktion (till exempel genom telefonrecept) är oacceptabelt.
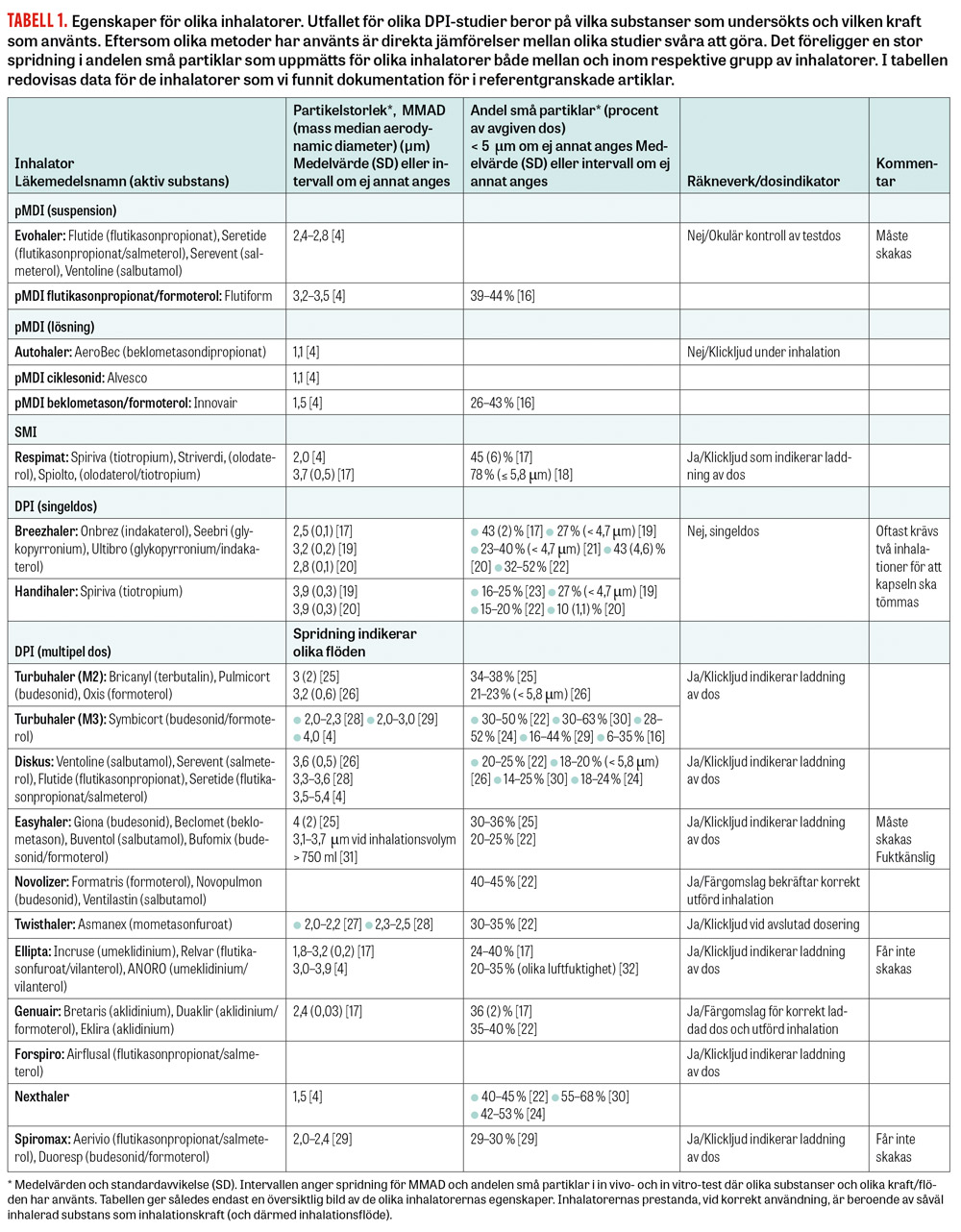
Tabell 1
Antalet personer med astma och KOL i Sverige överstiger en miljon, och de flesta patienter omhändertas inom primärvården. Läkemedel vid astma och KOL tillförs via inhalation, vilket innebär en rad fördelar framför systemisk administration. Inhalation leder läkemedlet direkt till målorganet där det tas upp och ger snabb effekt och minskad risk för systembiverkningar. Hur stor del av den dos som avges från inhalatorn som levereras till luftvägar och lungor bestäms både av produktrelaterade och patientrelaterade faktorer.
Inhalationstekniken är beroende av patientens förmåga att generera lämpliga inspiratoriska flöden, snabbheten med vilken inhalationen påbörjas, inhalationens duration och inhalationsvolymen [1, 2]. Förmågan att utföra en optimal inhalation varierar mellan personer, men även för samma individ beroende på aktuellt sjukdomsstatus och handhavande. Patientutbildning med instruktion i inhalationsteknik är därför av största vikt. Kunskapen om hur man använder en inhalator är färskvara. Många patienter som vid ett tillfälle kan utföra en korrekt inhalation gör ändå fel efter några månaders behandling. Inhalationstekniken måste därför kontrolleras vid varje besök av läkare eller astma/KOL-sjuksköterska. Vid behandling av obstruktiv luftvägssjukdom måste, förutom val av rätt läkemedel, även val av inhalator och patientens förmåga att använda inhalatorn korrekt beaktas [1].
Typer av inhalatorer
Antalet olika inhalatorer har ökat enormt på den svenska marknaden under senare år. Det finns inget sätt att på förhand avgöra vilken inhalator som passar bäst för en viss patient. Det är viktigt att utvärdera valet regelbundet och vid behov byta till en annan inhalator.
Inhalatorer för behandling av astma och KOL kan delas in i två huvudgrupper: inhalatorer som producerar en aerosol samt pulverinhalatorer. Inhalatorer med aerosol delas in i pMDI (pressured metered dose inhalers) samt SMI (soft mist inhalers). Pulverinhalatorer, DPI (dry powder inhalers), delas in i multidos- samt singeldosinhalatorer. I multidosinhalatorn matas doserna fram en och en. I singeldosinhalatorn laddas inhalatorn med en ny kapsel inför varje inhalation. En aerosolinhalator genererar ett moln av partiklar som ska inhaleras långsamt. Inhalation från en pulverinhalator måste tillföras energi för att deaggregera pulvret till små, inhalerbara partiklar. Detta kräver högre inandningsflöden än för aerosol.
Vid inhalation från pulverinhalatorer lämnar pulvret inhalatorn när inhalationen startar, varför samordning av inhalation och aktivering av inhalatorn inte krävs. Inhalation från pMDI och SMI kräver att aktiveringen av dosen koordineras med inhalationen. Användning av »spacer« (andningsbehållare) mellan inhalator och patient minskar behovet av koordination. Sprejen aktiveras och aerosolen levereras till spacern och inhaleras från denna.
För pMDI av typen »autohaler« aktiveras aerosolmolnet vid starten av inhalationen, vilket minskar koordinationsproblematiken. De nya HFA (hydrofluoroalkan)-sprejerna och SMI-aerosolerna lämnar inhalatorn med långsammare hastighet än de gamla freonsprejerna, vilket minskar betydelsen att använda spacer [3, 4]. En spacer kan förbättra inhalation av läkemedel hos patienter med mycket ytlig andning.
Lungdeponering
De viktigaste deponeringsmekanismerna för inhalationsläkemedel är impaktion och sedimentation. Impaktion innebär att partikeln av sin egen tröghet fortsätter rakt fram när luftvägen svänger och därmed når en yta (svalg, luftvägsdelningar) och fastnar. Stora partiklar impakteras därför ofta i svalg och övre luftvägar. Sedimentation innebär att partikeln faller nedåt på grund av gravitationen. Detta är anledningen till att man rekommenderar andhållning efter att inhalationen fullbordats. En aerosol består av droppar eller partiklar som är så små att de kan sväva i luft och som deponeras på slemhinnan i munhåla och luftvägar vid inhalation. Sannolikheten för att detta kommer att inträffa styrs av flera faktorer (Fakta 1). Egenskaper som partikelstorlek, andel små partiklar och den hastighet varmed en aerosol eller ett pulver lämnar inhalatorn är av betydelse för deponeringen. Även partiklarnas hygroskopicitet, svalganatomi och andningsmönster har betydelse. Deponering i både mun, svalg, trakea och bronker sker i huvudsak på grund av impaktion. I små luftvägar och den alveolära delen av lungan sker deponeringen via sedimentation.
Partikelhastighet och inhalationsduration
Aerosoler. Efter freonförbudet i slutet av 1980-talet bytte man från pMDI till pulverinhalatorer. I detta sammanhang introducerades nya aerosolinhalatorer som använde sig av freonfria drivgaser (norfluran, HFA-134a) eller inhalatorer som baseras på annan teknik för att generera aerosoler, till exempel SMI. I SMI trycksätts vätskan mekaniskt med hjälp av en fjäder som pressar ut vätskan med högt tryck så att ett moln bildas.
Optimalt vore att skapa ett stående moln av en aerosol från vilken patienten inhalerar. Detta eliminerar behovet av koordination mellan aktivering av inhalatorn och inhalationen och därmed risken för impaktion i svalg och övre luftvägar. För detta är det önskvärt att aerosolen lämnar inhalatorn med låg hastighet. [5].
Före inhalation av en aerosol ska patienten andas ut, helst till residualvolym, och därefter inhalera aerosolen långsamt. De viktigaste aspekterna vid inhalation av en aerosol från pMDI och SMI är koordination, lågt inspiratoriskt flöde (< 60 l/min), att inandningen är djup och att patienten håller andan under en tid så att partiklarna inte andas ut igen. Det vanligaste felet som patienter gör när de andas in en aerosol är för snabb inhalation [6].
Pulver. I pulverinhalatorer finns ingen drivgas utan dosen avges med hjälp av den kraft som genereras av patientens inhalation. Pulvret i inhalatorn slås sönder till små partiklar vid inhalationen. Kraften är en effekt av inhalationsflödet, och en multidosinhalator av reservoar- eller blistertyp kräver att patienten åstadkommer en kraftfull inhalation från början av inhalationen eftersom nedbrytningen till mindre partiklar sker i den initiala fasen av inhalationen [7]. Val av pulverinhalator måste anpassas efter patientens inhalationsprofil eftersom inhalatorerna har olika interna motstånd. Generellt gäller att inhalatorer med högt motstånd behöver lägre flöden än inhalatorer med lågt motstånd. För lågt inhalationsflöde för en given inhalator medför att inte hela läkemedelsdosen avges och att partiklarna inte deaggregeras, vilket ger ökad risk för impaktion i svalget. Vid för höga inhalationsflöden, speciellt genom pulverinhalatorer med lågt motstånd, ökar också risken för impaktion i svalg och övre luftvägar [6]. Pulverinhalatorer med högt motstånd tenderar att generera bättre lungdeposition med mindre variabilitet än pulverinhalatorer med lågt motstånd [7]. Vid svåra exacerbationer samt hos mycket unga och äldre patienter kan det vara svårt att generera tillräcklig inspiratorisk kraft för att leverera läkemedlet till lungorna från en pulverinhalator [6]. Hos vissa patienter med KOL-exacerbation och nedsatt inspiratoriskt flöde har risken för återinläggning visats vara större vid behandling med pulver- än med aerosolinhalator [8].
Förberedelse inför inhalation från en pulverinhalator och en aerosolinhalator innebär att patienten börjar med en maximal utandning. Optimal lungdeposition från en pulverinhalator är beroende av en kombination av inhalationsflöde, volym och accelerationshastighet [6]. Vid inhalation genom pulverinhalator ger låga flöden större partiklar medan högre flöden ökar risken för impaktion.
Inhalationsdurationen har framför allt betydelse för singeldosinhalatorer, men kan även ha betydelse för patienter med uttalad hyperinflation med kraftigt reducerad inspiratorisk kapacitet [6]. Rekommendation för denna typ av inhalator är att patienten inhalerar två gånger från samma kapsel för att tömma kapseln.
Hålla andan
Efter avslutad inandning bör patienten, oavsett inhalatortyp, hålla andan för att optimera effekten av läkemedlet. Att hålla andan möjliggör sedimentation av partiklarna som är tyngre än luft. Att hålla andan efter inhalation från en pMDI kan öka lungdepositionen, men det finns inga vetenskapliga studier som visat på förbättrad bronkdilatation eller andra långsiktiga konsekvenser. Eftersom det är möjligt att det är fördelaktigt att hålla andan föreslås en pragmatisk lösning med rådet att hålla andan minst 5 sekunder eller så länge som det känns bekvämt [9].
Partikelstorlek
Partikelstorleken anges oftast som den viktigaste parametern för hur effektiv en behandling med ett inhalerat läkemedel är [1]. I praktiken består läkemedelsaerosoler av partiklar med olika storlekar. Det vore möjligt att styra deponeringen mer effektivt om spridningen av storleksfördelningen för partiklar var mindre. Det finns många in vitro-metoder för att undersöka partikelstorleksfördelning från en inhalator. Det finns dock ingen generell modell som tar hänsyn till samtliga aspekter av de mycket komplexa förhållanden som definierar utfallet av en inhalation in vivo.
Den bästa kliniska effekten på lungfunktion observeras vid inhalation av partiklar med en diameter mellan 2 och 5 μm [1, 10]. Större partiklar (> 5 μm) deponeras i stor utsträckning i mun och svalg, och de minsta partiklarna (< 0,5 μm) deponeras inte i luftvägarna utan följer med utandningsluften [10].
Aerosolinhalatorer producerar en konstant mängd partiklar av en viss storlek, medan storleken på inhalerade partiklar från en pulverinhalator är beroende av inhalationsflödet och inhalatorns interna motstånd, vilket avgör graden av deaggregering och därmed den slutliga partikelstorleken.
Enligt det europeiska regelverket som styr läkemedelstillverkning är en tillverkare av inhalatorer/inhalationsläkemedel skyldig att utföra ett antal test för att mäta partikelstorlek, partikelstorleksfördelning, andelen finpartiklar etc, för att bekräfta att inhalatorn levererar enligt förutbestämda definierade nivåer vid olika flödeshastigheter (Tabell 1).
Uppmätt och levererad dos
Med uppmätt dos avses den dos av ett läkemedel som faktiskt finns i inhalatorn, och med levererad dos avses den dos som faktiskt når patienten. Skillnaden mellan dessa doser är andelen av läkemedlet som fastnar i inhalatorn. Majoriteten av inhalatorerna levererar mellan 75 och 90 procent av uppmätt dos till patienten.
Handhavande av inhalatorer
Det finns ett flertal faktorer som påverkar funktionen hos en inhalator. Vissa pulverinhalatorer är fuktkänsliga och vissa måste skakas, medan andra inte får skakas innan inhalationen genomförs. Vissa aerosolinhalatorer som innehåller suspension måste skakas före inhalation. Vissa pulverinhalatorer är lägeskänsliga eller så lämnar inte pulvret doskammaren om inhalatorn inte hålls upprätt efter laddning av dosen. Singeldosinhalatorer (kapselinhalatorer) kräver god inandningsvolym (ofta två inhalationer) för att kapseln ska tömmas helt.
Samtliga multidosinhalatorer och SMI har räkneverk med olika signaler för att patienten ska kunna se hur många doser som finns kvar i inhalatorn (Tabell 1). Dessa signaler kan vara värdefulla för behandlingsresultatet.
Sammanfattningsvis gäller att faktorer som laddning av dos, position av inhalator, skakning/inte skakning, grad av utandning före inhalation, inandningsflöde, inandningskraft, inandningsduration, förvaring i fuktig miljö och användning av spacer är viktiga för ett korrekt handhavande av inhalatorer. Singeldosinhalatorer kräver mer förberedelser före inhalation än multidosinhalatorer, pMDI och SMI.
Patientpreferenser
Flera studier har undersökt patienters inhalatorpreferens. Det finns dock inget utvärderat verktyg för att kartlägga denna typ av information. Olika parametrar har bedömts som viktiga i olika studier. Behandlingen måste därför bedömas utifrån kliniska utfallsmått.
Inlärningsaspekter
Instruktion, träning och kontroll av inhalationsteknik är viktigt och har mycket hög prioritet i Socialstyrelsens nationella riktlinjer för vård vid astma och KOL (Socialstyrelsen; 2015). Vid otillfredsställande behandlingsresultat ska inhalationsteknik och handhavande av inhalatorn kontrolleras före byte av läkemedel eller ökning av dos.
Ofrivilligt byte av inhalator
För inhalationsläkemedel åligger det vårdgivaren att se till att patienten får tillräcklig instruktion och kunskap för att kunna inhalera korrekt från den förskrivna inhalatorn och därmed tillgodogöra sig läkemedlet. Risken att göra fel vid inhalationen med åtföljande försämrad sjukdomskontroll ökar om patienten använder olika (särskilt olika typer av) inhalatorer [11]. Förskrivning av pulverinhalator och aerosolinhalator till en och samma patient ska undvikas. Ofrivilligt byte innebär att patienter känner sig otrygga med sin behandling och är associerat med större risk att göra fel. Frånsett att läkemedlet inte når målorganet påverkas förtroendet för medicinen och följsamheten blir sämre [11, 12].
I Sverige är det i dag inte tillåtet för apoteken att byta inhalator men i Norge kan apotekaren fritt byta pulverinhalator utan att informera behandlande läkare. I en italiensk studie visades att inhalatorbyte på apotekets initiativ resulterade i ökade handhavandefel. Förtjänsten på en något billigare inhalator konsumerades av ökade sjukvårdskostnader med akuta besök och behov av sjukhusvård på grund av försämrad sjukdomskontroll. Man har beräknat att ett kritiskt handhavandefel hos 100 patienter med KOL och 100 patienter med astma ger en merkostnad för sjukvården på 68 000 euro/år [13]. Bedömning av inhalerade läkemedel måste bedömas baserat på ingående substans(er) och inhalator. Det är oacceptabelt att bortse från inhalatorns betydelse. Byte av inhalator försämrar ofta behandlingsresultat [14] och måste föregås av noggrann instruktion angående användning av den nya inhalatorn. Därför är det tveksamt att utfärda centrala påbud, till exempel i ett landsting, om användning av en viss inhalator. Dessvärre förnyar många patienter med astma och KOL sina recept på inhalationsläkemedel genom telefonsamtal med mottagningen utan att besöka läkare eller sjuksköterska [15]. Många patienter klarar inte av att använda sin vanliga inhalator, och följden av ett okontrollerat inhalatorbyte (till exempel via telefonsamtal) kan bli förödande.
Val av inhalator
Det finns inga patientegenskaper eller andra faktorer som kan vägleda inhalatorvalet inför start av inhalationsbehandling. Användningen skiljer sig mycket mellan olika inhalatorer (se ovan) och framför allt mellan olika inhalatortyper (pulverinhalator vs pMDI/SMI). Om en inhalator används på ett korrekt sätt så finns det dock goda förutsättningar att behandlingen ska fungera. Här skulle en nationell lista över befintliga läkemedel–inhalatorkombinationer kunna vara till hjälp. En kortfattad nationell kravspecificerad beskrivning av för- och nackdelar med varje produkt skulle ge ett underlag för varje läkare att skaffa sig en mer ingående uppfattning om några få inhalatorer av varje typ och att använda dessa i första hand. Om behandlingen kräver ytterligare korrigering kan ju detta göras genom mer ingående studium av listan eller i samråd med mer erfaren kollega, astma/KOL-sjuksköterska på vårdcentralen eller med en lung- och allergispecialist. Vid otillfredsställande behandlingsresultat ska inhalatorbyte (ofta till en annan inhalatortyp eller ibland till en annan inhalator av samma typ) övervägas. På detta sätt kan man titrera fram vilken läkemedel–inhalatorkombination som passar en viss patient bäst. Målsättningen är att patienten har så få olika inhalatorer som möjligt och att en och samma patient inte har olika inhalatortyper (till exempel pMDI och pulverinhalator).
Läs även:
Potentiella bindningar eller jävsförhållanden: Kjell Larsson har de senaste fem åren deltagit i rådgivningsgrupper och/eller engagerats som föredragshållare och/eller deltagit i utbildningsaktiviteter arrangerade av Astra Zeneca, Boehringer Ingelheim, Glaxo Smith Kline, Chiesi, Novartis, Orion, Takeda och Teva; Leif Bjermer har de senaste fem åren deltagit i rådgivningsgrupper och/eller engagerats som föredragshållare och/eller deltagit i utbildningsaktiviteter arrangerade av ALK, Astra Zeneca, Boehringer Ingelheim, Chiesi, Glaxo Smith Kline, Novartis och Teva; Magnus Svartengren har de senaste fem åren deltagit i rådgivningsgrupper och/eller engagerats som föredragshållare arrangerade av Astra Zeneca, Boehringer Ingelheim, Chiesi, Glaxo Smith Kline, Meda, Novartis och Teva.
Fakta 1. Faktorer som styr deponering av inhalerade läkemedel i luftvägarna
Inhalatoregenskaper
- Partiklarnas aerodynamiska diameter
- Distribution av storleksfördelning
- Andel små partiklar
- Partikelhastighet under inhalationen
- Partikelform
- Partikelladdning
- Hygroskopicitet
Patientfaktorer
- Luftvägsgeometri (grad av obstruktion)
- Anatomiska variationer i svalget
- Funktionella svalgförändringar (stämbandspares, obesitas)
- Andningsmönster
- Inhalationskraft
- Handhavandefel