Bröstsmärta står för ca 5 procent [1] av alla akutbesök och kan orsakas av ett flertal olika tillstånd. Vi presenterar en handläggningsalgoritm för att bedöma sannolik diagnos, avgöra om en patient behöver läggas in eller kan skrivas hem från akuten och föreslår lämplig utredning. En viktig fråga är om det kan vara kranskärlssjukdom, lungemboli eller akut aortasyndrom [2] som orsakar patientens symtom.
Strukturerad handläggning av patienter med bröstsmärta kan sannolikt bidra till minskad belastning på sjukhusets vårdavdelningar och förhindra onödiga utredningar. I en optimerad handläggning av patienter med bröstsmärta är också förkortad handläggningstid på akutmottagningen central. Detta blir allt viktigare, eftersom belastningen på våra akutmottagningar ständigt ökar.
Orsaker till bröstsmärta
Eftersom afferenta nervbanor från hjärta, lungor, de stora torakala kärlen och matstrupen förlöper till samma autonoma ganglier [3] kan en mängd kardiella och icke-kardiella tillstånd orsaka likartad bröstsmärta [4]. 5–10 procent av patienter med hjärtinfarkt har ingen bröstsmärta och 5–10 procent upplever endast lindrigt obehag i bröstet [5]. Endast 5 procent [6] av alla som söker med bröstsmärta på akuten har hjärtinfarkt.
Akut kranskärlssjukdom är dock den dominerande orsaken till farlig bröstsmärta hos patienter som söker akutmottagningen. Prevalensen av farliga orsaker till bröstsmärta är starkt beroende av ålder [7-10] och kön [8-10]. Man bör därför utgå från »pre-test probability«, dvs sannolikheten att en undersökning ska vara positiv, vid beslut om lämplig diagnostik och handläggning. Mycket talar för att risken för vårdskador är större än risken att missa viktig diagnos hos många lågriskpatienter [11].
Ett ovanligt men omedelbart livshotande tillstånd som debuterar med bröstsmärta är torakal aortadissektion [12].
Läkarens uppgift
Viktiga uppgifter på akutmottagningen är att
- identifiera potentiellt livshotande tillstånd genom värdering av symtom och vitalparametrar
- fokusera på akut kranskärlssjukdom, eftersom det är 3–4 gånger vanligare bland patienter med bröstsmärta än summan av andra farliga diagnoser som aortadissektion, pneumotorax, myokardit och lungemboli [7]
- utesluta andra viktiga differentialdiagnoser som akut perikardit, esofagussjukdom och ulkus, om akut kranskärlssjukdom bedöms mindre sannolik
- avgöra om patienten behöver läggas in
- besluta om lämplig utredning.
Typisk ischemisk bröstsmärta karakteriseras av retrosternal känsla av tryck eller tyngd (angina) som strålar ut i armarna eller hals/käke; smärtan är intermittent med flera minuters duration eller ihållande [13]. Utstrålning till vänster arm ökar inte sannolikheten för myokardischemi [14].
Anamnesen används för att särskilja stabil och instabil angina. Instabil angina definieras som myokardischemi i vila eller vid minimal ansträngning utan signifikant myocytnekros [13]. Instabil angina misstänks när något av följande föreligger:
- viloangina >20 minuter
- nydebuterad angina som ger lindrig till uttalad begränsning av alldagliga aktiviteter
- crescendoangina, dvs nyligen destabiliserad stabil angina som ger uttalad påverkan på alldagliga aktiviteter
- postinfarktangina, dvs recidiverande angina inom 30 dagar efter hjärtinfarkt.
Strukturerad handläggning
Hemodynamiskt påverkade patienter
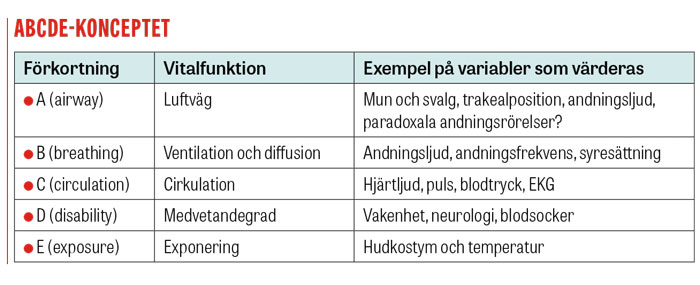
Påverkade patienter handläggs initialt enligt ABCDE-konceptet [15]. Patienter med tecken på chock stabiliseras, och etiologin eftersöks. Ultraljudsdiagnostik med RUSH-protokollet (rapid ultrasound for shock and hypotension) bör normalt genomföras [16, 17]. Patienter med plötsligt påkommen bröstsmärta, ofta beskriven som det värsta patienten har upplevt, ska utredas med akut DT-undersökning av aorta för att utesluta aortadissektion. Patienter med svår dyspné som inte förklaras av hjärtsvikt bör genomgå DT-undersökning för akut lungemboli, och patienter med persisterande ST-höjningar på EKG bör skyndsamt undersökas med koronarangiografi.
Patienter utan hemodynamisk påverkan
Vitalparametrar används för bedömning av sjukdomsgrad, men även för etiologisk vägledning. Flera samtidigt påverkade vitalparametrar, sänkt medvetandegrad, hög andningsfrekvens och hypoxi indikerar dålig prognos [18]. Låg syresättning kan tala för lungemboli, pneumoni eller lungödem, men är också vanlig vid t ex kroniskt obstruktiv lungsjukdom. Sinustakykardi kan ses vid ett stort antal tillstånd, inklusive lungemboli och infektionssjukdomar. Hypertoni kan indikera hypertensivt lungödem eller katekolaminpåslag på grund av stress eller smärta vid t ex aortadissektion. Feber kan finnas vid pneumoni, men förekommer vid all infektionssjukdom och ibland vid lungemboli.
EKG-bedömning
EKG utgör basen vid diagnostisering av ST-höjningsinfarkter (STEMI) [19]. EKG är dock normalt i över en tredjedel av fallen vid icke-ST-höjningsinfarkter (NSTEMI) [7, 13].
Ett normalt EKG tillsammans med omätbart troponin T analyserat med Roches högkänsliga metod eller omätbart troponin I analyserat med Abbots högkänsliga metod utesluter hjärtinfarkt med hög säkerhet [20]. Vilo-EKG har begränsat värde i diagnostiken [21] av lungemboli, men T-vågsnegativitet eller sinustakykardi förekommer i 25–30 procent av fallen [22]. Vid perikardit ses ofta PQ-sänkning och/eller utbredda ST-höjningar [23]. Minskad elektrisk amplitud med elektrisk alternans kan indikera hjärttamponad, men uppkommer sent i förloppet [23]. EKG kan även påvisa komplikationer till hjärtinfarkt som ventrikeltakykardi och AV-block.
Lågriskpatienter med instabil angina kan, om de förblir smärtfria, handläggas som vid stabil angina förutsatt att EKG är normalt [24].
Anamnes
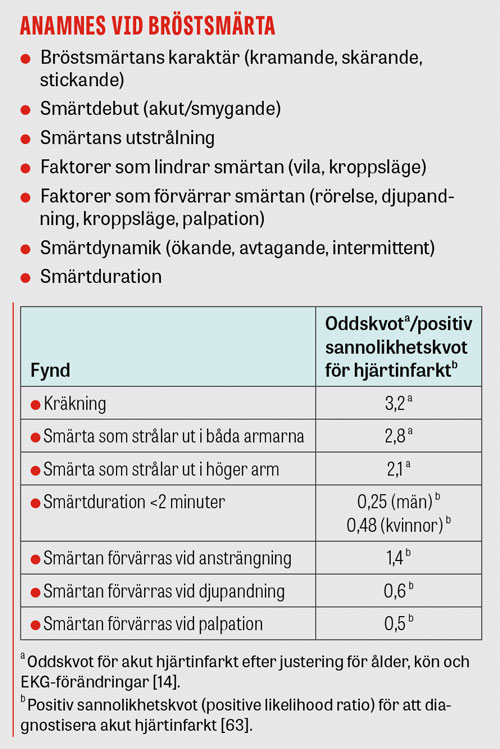
Vid anamnesen är det viktigt att efterfråga bröstsmärtans karaktär [14]. Bröst-, rygg- eller magsmärta med abrupt insättande, kraftig intensitet och/eller slitande/rivande karaktär ökar sannolikheten för akut aortasyndrom [2].
Associerade symtom kan ge diagnostisk vägledning:
- dyspné kan tala för pneumoni, hjärtsvikt och lungemboli; plötsligt insättande dyspné är det vanligaste förekommande symtomet vid lungemboli
- pleuritsmärta är i regel associerad med godartade tillstånd, men förekommer även vid pneumoni, lungemboli [25] och perikardit
- svimning är associerad med lungemboli, aortadissektion och arytmi till följd av myokardischemi.
Förekomst av riskfaktorer ökar inte sannolikheten för hjärtinfarkt, med undantag för rökning [26-29]. I multivariat analys är endast troponin T, ischemitecken på EKG, synlig kallsvett, hypotoni definierad som systoliskt blodtryck <100 mm Hg, smärtutstrålning till höger arm/axel och crescendoangina [26] associerat med pågående hjärtinfarkt. Bindvävssyndrom, hereditet för aortasjukdom, känd aortaklaffsjukdom och tidigare aortamanipulation, t ex operation av aortaaneurysm eller byte av aortaklaff, ökar sannolikheten för akut aortasyndrom [2].
Status
Hjärtauskultation kan avslöja dels oregelbunden rytm, som vid förmaksflimmer, dels olika klaffvitier som ger bröstsmärta eller har orsakats av hjärtinfarkt, t ex akut mitralisinsufficiens eller ventrikelseptumdefekt, dels gnidningsbiljud vid perikardit. Torakal aortadissektion kan engagera klaffplanet och ge upphov till akut aortainsufficiens. Rassel över lungfälten kan indikera pneumoni eller lungödem.
Vid misstanke om akut aortasyndrom kompletteras status med perifera pulsar och blodtryck i båda armarna. Dessa undersökningar kan dock inte utesluta akut aortasyndrom, och värdet av dessa kliniska fynd för handläggningen är oftast begränsat. Bröstsmärta i kombination med akut neurologiskt bortfall talar starkt för akut aortasyndrom [2].
Halsvenstas indikerar förhöjt centralt ventryck och kan ibland ses vid akut lungemboli, tamponad eller högerkammarsvikt. Blodtrycksstegring kan tala för hypertensivt lungödem och lågt blodtryck kan tala för chock, t ex vid aortadissektion. Ensidig bensvullnad eller bensmärta kan tala för djup ventrombos och/eller lungemboli [30, 31].
Provtagning
CRP-stegring ses vid pneumoni, men kan även förekomma vid lungemboli, aortadissektion och hjärtinfarkt.
Vid stark klinisk misstanke om lungemboli (Wells-poäng >4) ska inte D-dimer analyseras, utan bilddiagnostik ska påbörjas direkt. PERC-negativa (pulmonary embolism rule-out criteria) patienter, som har en mycket liten risk för lungemboli, ska inte heller testas med D-dimer [32]. D-dimer ska således kontrolleras för att utesluta lungemboli om Wells-poäng är ≤4, men patienten ändå anses ha risk för lungemboli [33]. Om Wells-poäng är ≤4 behövs alltså ingen ytterligare lungembolidiagnostik om D-dimer är negativ [34]. Vissa författare rekommenderar vidare åldersjustering av D-dimergränsen [32] för att reducera behovet av bilddiagnostik. PERC-regeln ska enbart tillämpas om läkaren aktivt misstänker lungemboli men risken bedöms som mycket låg.
Vid svag klinisk misstanke om aortadissektion, icke-breddökat mediastinum på lungröntgen och transtorakalt hjärtultraljud utan aortavidgning kan D-dimer även användas för att utesluta aortadissektion [2].
Troponiner bör kontrolleras enbart om det finns en rimlig klinisk misstanke om hjärtinfarkt eller för att värdera myokardpåverkan vid misstänkt perimyokardit. Bland patienter med bröstsmärta utan hjärtinfarkt har minst 20 procent troponinnivåer över den 99:e percentilen när man använder de nya högkänsliga troponinmetoderna [35, 36]. Hög troponinnivå [37] och/eller stor troponindynamik ökar sannolikheten för hjärtinfarkt, men 26 procent av alla patienter med hjärtinfarkt har troponindynamik <20 procent under 6 timmars observation [38]. Troponin stiger 2 till 4 timmar efter symtomdebut [39], varför patienter som provtas tidigt teoretiskt kan ha låga troponinnivåer trots pågående hjärtinfarkt.
Smärta i kombination med akut njurskada (akut försämring av njurfunktion) kan tala för akut aortasyndrom [2].
Vid klinisk misstanke om icke-kardiell genes får komplettering med riktad provtagning övervägas om det inte redan gjorts som del i akutmottagningens standardprovtagning.
Bedside-ultraljud
Undersökning med bedside-ultraljud bör genomföras vid hemodynamisk påverkan. Även icke-kardiologer kan relativt enkelt lära sig att bedöma perikardvätska [40], vänsterkammarfunktion [41], pleuravätska [40], lungödem [42] och pneumotorax [43].
Preliminärdiagnos utifrån flödesschema
Omhändertagande av patienter med bröstsmärta underlättas genom användning av ett diagnostiskt flödesschema.
Inläggning
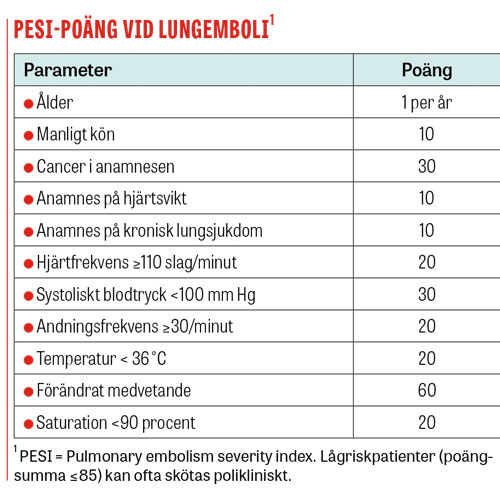
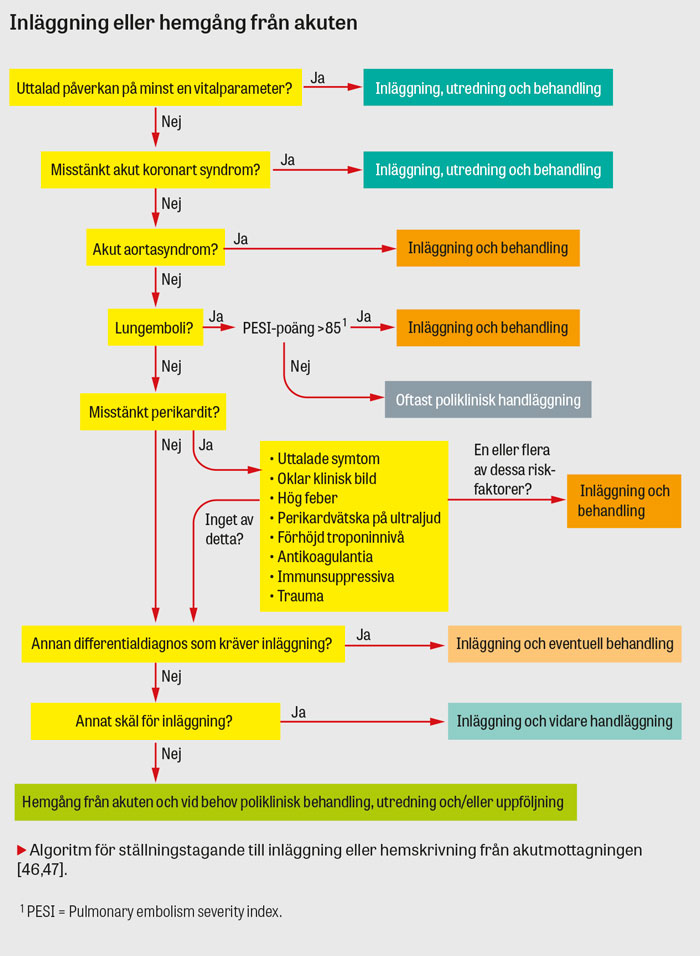
Patienter med hjärtinfarkt, instabil angina och aortadissektion ska alltid vårdas inneliggande på sjukhus. Torakal aortadissektion är ett urakut tillstånd som kräver omedelbar transport till toraxkirurgiskt centrum för operation. Vid all angina bör en riskbedömning göras [44, 45]. Patienter med lungemboli [46] och PESI-poäng (Pulmonary embolism severity index) ≤85 har mycket god prognos och kan handläggas polikliniskt. De flesta patienter med perikardit behöver inte läggas in på sjukhus. Uttalade symtom, oklar klinisk bild eller hög feber, ultraljudsfynd med perikardvätska, myokarditinslag, antikoagulationsbehandling, immunsuppressiv behandling eller trauma motiverar dock inläggning [47].
Högkänsligt troponintest ger snabbare bedömning av patienter med bröstsmärta på akuten och har reducerat antalet inläggningar av patienter med bröstsmärta med 36 procent under de 4 första årens användning på Karolinska universitetssjukhuset, Huddinge [48]. Prognosen för patienter med bröstsmärta utskrivna från akuten förbättrades också efter införandet av högkänsligt troponin T-test [49].
I en studie från USA kunde man visa att rutinmässig undersökning av patienter med bröstsmärta med DT-kranskärl kan minska inläggningar [50] till priset av fler koronarangiografier. Användning av ett flödesschema kan underlätta beslut om inläggning eller hemskrivning från akuten [46, 47].
Diagnostik efter akutmottagningen
Arbetsprov
Arbetsprov bör inte göras hos patienter med hög sannolikhet för koronarsjukdom på grund av risk för falskt negativt resultat [24]. Positivt prediktivt värde är 75 procent och negativt prediktivt värde 84 procent för kranskärlssjukdom [51]. För att bedöma sannolikheten för kranskärlssjukdom måste arbetsprovet värderas tillsammans med bl a ålder och kön [52]. Tabeller finns för att översätta watt på ergometersystem till metabola ekvivalenter (MET) [53] om man vill värdera risk med den europeiska kardiologföreningens riktlinjer. Riskvärdering kan även ske med treadmill-poäng [54].
Lågriskpatienter med arbetsprov utan ischemitecken kan skrivas hem från akuten om de erbjuds poliklinisk uppföljning [55].
Stressekokardiografi
Indikationen för stressekokardiografi är intermediär sannolikhet för kranskärlssjukdom. Regionalt nedsatt systolisk väggförtjockning på hjärtultraljud efter provokation med läkemedel eller med liggande cykling har hög specificitet för kranskärlssjukdom [56]. Sensitiviteten för >50-procentig luminal kranskärlsstenos är ca 80–85 procent [56]. Obesitas och kroniskt obstruktiv lungsjukdom kan omöjliggöra en konklusiv undersökning.
Myokardskintigrafi
Indikationerna för myokardskintigrafi [57] är intermediär sannolikhet för kranskärlssjukdom, avvikande vilo-EKG med icke-specifika ST–T-förändringar, vänsterkammarhypertrofi eller ledningshinder, eller icke-diagnostiskt arbetsprov där patienten uppnår mindre än 85 procent av förväntad maximal hjärtfrekvens eller har pågående digoxinbehandling som gör bedömning av ST–T-sträckan svår. Akut myokardskintigrafi för att utesluta akut kranskärlssjukdom erbjuds från akutmottagningen på en del centrum [58].
DT-kranskärl
Studier har visat att DT-kranskärl hos symtomatiska patienter med misstänkt koronarsjukdom inte ger bättre kliniskt utfall än enbart funktionell testning [59, 60]. Studierna inkluderade inte någon kontrollgrupp som inte genomgick någon testning. Patienter med negativa undersökningsfynd vid DT-kranskärl kan, enligt amerikanska studier, skrivas ut från akuten [61, 62]. Det är oklart om detsamma gäller i Sverige.
De flesta med hjärtinfarkt bör kranskärlsröntgas
De flesta med hjärtinfarkt [13, 19] bör kranskärlsröntgas, undantaget är mycket sköra patienter. Pågående infektion gör ibland att angiograförerna vill avvakta. Det saknas riktlinjer för hur patienter med typ 2-hjärtinfarkt ska utredas.
Potentiella bindningar eller jävsförhållanden: Martin J Holzmann har mottagit konsultarvoden från Pfizer och Actelion. Ola Hammarsten har mottagit arvoden från AstraZeneca.