Vaskulärt Ehlers–Danlos syndrom (VED) är en mycket ovanlig, autosomalt dominant nedärvd, sjukdom. Endast ca 50 individer i Sverige har en molekylärgenetiskt verifierad diagnos.
En randomiserad studie visar att
betablockeraren celiprolol kan förebygga kärlkatastrofer vid vaskulärt Ehlers–Danlos syndrom.
Vid kärlkomplikationer är konservativ behandling första val, men det kan vara riskabelt att avstå från öppen eller endovaskulär kärlkirurgi.
Behandling behöver ofta inledas omgående, men kontakt bör tas med ett center med erfarenhet av att behandla detta farliga och ovanliga tillstånd.
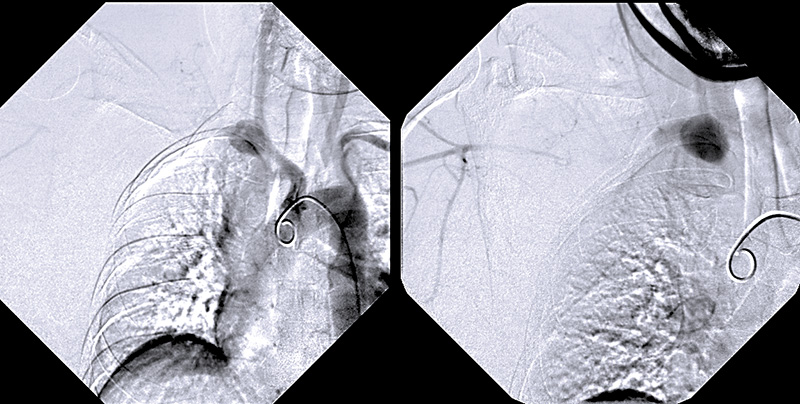
Figur 1. Angiografibilder som visar hur ett pseudoaneurysm, sekundärt till en artärruptur, fyller sig i början av arteria subclavia (t v). Senare fyller sig arteria axillaris via kollateraler, medan kontrasten dröjer kvar i pseudoaneurysmet (t h).
Den vaskulära formen av Ehlers–Danlos syndrom (VED) är en ovanlig ärftlig sjukdom; endast ca 50 personer i Sverige är drabbade. Sjukdomen är autosomalt dominant nedärvd, och beror på en heterozygot mutation i genen som kodar för prokollagen typ 3 (COL3A1). Mutationen leder till uttalad kärlskörhet med risk för artärrupturer och aneurysm. Patienterna får lätt blåmärken även vid mindre trauma, och det blöder ofta när de borstar tänderna. De är nästan alltid för tidigt födda, eftersom fosterhinnorna är sköra. Typiskt är en s k skomakartumme, överextension av tummens grundled. Hypermobiliteten är ofta begränsad till små leder i händerna, men man ser sällan generell överrörlighet som vid vanligare former av Ehlers–Danlos syndrom (EDS). Spontana rupturer av esofagus, kolon och uterus förekommer, liksom stora lacerationer av förlossningskanalen, särskilt när en drabbad kvinna föder ett friskt, och därmed oftast fullgånget barn [1, 2].
Vi använder medvetet inte förkortningen EDS för denna patientgrupp, utan i stället VED, eftersom vi vill betona de mycket speciella och potentiellt livshotande problem som den lilla gruppen med vaskulärt Ehlers–Danlos syndrom har. Även om få drabbas är det viktigt att läkare inom olika specialiteter känner till sjukdomen. Den stora andel av patienterna som har nymutationer har ofta inte blivit diagnostiserade, och konsekvenserna av en felbehandling är ofta katastrofala.
Sedan många år tillbaka har kärlkirurger, angiologer och kliniska genetiker i Uppsala intresserat sig för denna lilla men svårt drabbade patientgrupp [3]. Vi har nyligen genomfört en systematisk litteraturgenomgång av alla fallbeskrivningar och små fallserier som finns publicerade i litteraturen [4]. Totalt identifierades 231 patienter bland vilka 119 har behandlats under perioden 1997–2010. All operativ behandling av patienter med vaskulärt Ehlers–Danlos syndrom, såväl med öppen som med endovaskulär kirurgi, är förenad med stora risker, men det kan också vara riskabelt att avstå från behandling. All planerad invasiv behandling bör ske på en enhet med erfarenhet av patientgruppen.
Ny läkemedelsbehandling prövad i randomiserad studie
Debutsymtomet vid vaskulärt Ehlers–Danlos syndrom hos tidigare asymtomatiska individer är ofta en arteriell kärlkatastrof. Aortadissektion är särskilt fruktad. Man har observerat en minskad intima–mediatjocklek, associerad med ökad mekanisk stress och risk för ruptur av den försvagade kärlväggen.
För att minska risken för arteriella komplikationer skulle en möjlighet vara att sänka ett förhöjt blodtryck, minska hjärtfrekvensen, och därigenom minska pulstryck och mekanisk stress. Vid genomförandet av en randomiserad behandlingsstudie (BBEST-studien) valdes betablockeraren celiprolol. Celiprolol har både B1-blockerande och B2-stimulerande effekter, vilket leder till minskad mekanisk stress på kollagena strukturer i kärlväggen [5].
Studien genomfördes i Belgien och Frankrike på 53 patienter med kliniskt vaskulärt Ehlers–Danlos syndrom, varav 33 hade en molekylärgenetiskt påvisad mutation. Patienterna randomiserades till aktiv behandling eller kontrollgrupp. Den aktiva gruppen (25 patienter) fick celiprolol 100 mg/dag som upptitrerades var sjätte månad med 100 mg/dag till en maximal dos av 400 mg/dag. Kontrollgruppen fick ingen aktiv behandling.
Den primära utfallsvariabeln var arteriell ruptur eller dissektion, den sekundära tarm- eller uterusruptur. Studien planerades fortgå i fem år men avbröts efter 47 månader pga en signifikant behandlingsvinst i den aktiva gruppen. Då hade 50 procent drabbats av arteriell ruptur eller dissektion (det primära utfallet) i kontrollgruppen, jämfört med 10 procent i behandlingsgruppen. Den absoluta riskreduktionen var 64 procent för primärt och 69 procent för sekundärt utfall.
Receptorblockerare med agonistisk effekt
Celiprolol är en kardioselektiv B1-receptorblockerare med agonistisk effekt på B2-receptorn. Hos hypertensiva individer ger celiprolol en blodtryckssänkning, men ej hos normotensiva. I BBEST-studien sågs ingen sänkning av blodtryck och pulstryck i den aktivt behandlade gruppen, då de flesta i gruppen var normotensiva vid studiestart. Celiprolol tros ha en stabiliserande hemodynamisk effekt genom att förhindra excessiva puls-och blodtrycksstegringar även i den normotensiva gruppen.
TGF-β (transformerande tillväxtfaktor beta) är en familj av cytokiner som i olika sammanhang har skilda effekter vid utveckling av kärlsjukdom, och ofta motsatta funktioner vid olika tillstånd. TGF-β är en viktig tillväxtfaktor vid sårläkning, och är nödvändig för kollagensyntes och fibrotisering. TGF-β tycks därför ha en kärlskyddande och även antiinflammatorisk effekt i kärlväggen [6, 7], och har experimentellt visats kunna stabilisera aortaaneurysm hos råtta [8].
Denna effekt skulle teoretiskt kunna förklara en minskad risk för aneurysmutveckling och kärlbristning vid vaskulärt Ehlers–Danlos syndrom, eftersom det finns ett starkt samband mellan adrenerg β2-receptor och TGF-β-påverkan, där man ser ett ökat uttryck för TGF-β vid stimulering av receptorn [9]. TGF-β kan öka produktionen av kollagen typ I och typ III, vilket leder till fibrotisering [10]. Det är tänkbart att kronisk β2-stimulering ökar kollagensyntesen genom ökat uttryck för TGF-β, vilket skulle kunna förklara en del av den positiva effekten av celiprolol i BBEST-studien.
Preliminära erfarenheter av celiprolol i Uppsala
Vid direktkontakt med ansvarig för BBEST-studien i Paris har upptitreringen av celiprolol modifierats till att nå måldosen 400 mg/dag inom 1–2 månader. Vid Akademiska sjukhuset, Uppsala, har nio patienter påbörjat behandlingen. I två fall har viss bradykardi förhindrat upptrappning till full dos. I övrigt har inga subjektiva eller objektiva bieffekter av behandlingen noterats.
Öppen kirurgisk och endovaskulär behandling
Det är svårt att studera behandlingen av denna ovanliga sjukdom. Ett sätt är att sammanställa fallbeskrivningar och mindre serier i litteraturen [3, 4]. Denna metod är dock problematisk. Publikationsbias kan ge ett urval av spektakulära eller lyckade fall. Inte ens under perioden 1996–2010 var fler än 24 procent av de publicerade fallen (29 av 119) molekylärgenetiskt verifierade [4]. En del fall kan därför gälla andra tillstånd än vaskulärt Ehlers–Danlos syndrom, exempelvis det relativt nyligen beskrivna Loeys–Dietz syndrom [11], ett autosomalt dominant nedärvt tillstånd som beror på en mutation i TGF-β-receptorn, typ 1 eller typ 2, som först beskrevs år 2005.
Totalt identifierades 231 patienter, jämnt fördelade mellan könen. I 40 procent av fallbeskrivningarna hade patienterna behandlats för (ofta multipla) aneurysm. Hos 33 procent noterades en primär kärlruptur, och 18 procent hade en karotido-kavernös fistel. Mortaliteten var något lägre efter endovaskulär än efter öppen kirurgi (24 respektive 30 procent). Det är svårt att dra några säkra slutsatser av detta fynd, eftersom grupperna inte nödvändigtvis är jämförbara. De patienter som avled var i genomsnitt 31 år gamla, och det finns en del osäkra data som tyder på att risken för kärlkatastrof skulle vara störst (och därmed att indikationen för profylax med celiprolol är som starkast) i åldern 20–40 år. Möjligen blir blodkärlen styvare och mindre rupturbenägna med ökande ålder.
Angiografi har ansetts vara i det närmaste kontraindicerat vid vaskulärt Ehlers–Danlos syndrom eftersom både artärruptur och trombos är vanliga följeslagare om sedvanlig teknik används vid punktion av dessa sköra blodkärl. Den säkraste tekniken vid artär- och venpunktion av patienter med vaskulärt Ehlers–Danlos syndrom är att frilägga kärlet och punktera under uppsikt, och att sedan försluta med både sutur och vävnadslim. Det är möjligt att denna uppfattning får omprövas med modern ultraljudsstyrd punktionsteknik, förutsatt att särskild omsorg iakttas. Det kommer allt fler färska rapporter om framgångsrik endovaskulär behandling av patienter med vaskulärt Ehlers–Danlos syndrom [12, 13].
Det kliniska beslutsfattandet kring patienterna är ofta svårt. Även om konservativ behandling ofta är det bästa alternativet kan det straffa sig att inte vara tillräckligt aktiv. Vi upplevde detta starkt för några år sedan när vi behandlade en tidigare odiagnostiserad kvinna som drabbats av ruptur av arteria subclavia i samband med sin första förlossning (Figur 1). Medan vi trycksänkte patienten och konfererade om vi skulle behandla henne endovaskulärt eller öppet avled hon plötsligt då det 10 dagar gamla pseudoaneurysmet brast in i pleura [14]. Diagnosen vaskulärt Ehlers–Danlos syndrom misstänktes på kliniska grunder, men kunde ställas molekylärgenetiskt först efter denna tragiska händelse.
Molekylärgenetisk diagnostik
Vid misstanke om vaskulärt Ehlers–Danlos syndrom konfirmeras diagnosen med en hudbiopsi för odling av fibroblaster, på vilka biokemisk analys utförs. Om denna visar ett avvikande mönster går man vidare med molekylärgenetisk analys av COL3A1-genen. Om misstanken om vaskulärt Ehlers–Danlos syndrom är stark, men den biokemiska analysen inte påvisar något avvikande mönster, bör man ändå gå vidare med genetisk diagnostik, då en viss typ av mutationer (nollmutationer) inte behöver ge ett avvikande biokemiskt mönster [15]. Man har dock nyligen börjat göra omvänd diagnostik, dvs att molekylärgenetisk analys utförs primärt. Om denna inte påvisar mutation, men misstanke om vaskulärt Ehlers–Danlos syndrom kvarstår, tas en hudbiopsi för biokemisk analys.
Konklusion
Svåra kärlkomplikationer vid vaskulärt Ehlers–Danlos syndrom har tidigare inte säkert kunnat förebyggas med specifik behandling. Mycket talar nu för att man genom behandling med celiprolol kan förebygga kärlkomplikationer. Aktiv behandling med öppen eller endovaskulär kirurgi är riskfylld, men kan också vara livräddande i utvalda fall.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.