Antikroppsantidoten idarucizumab kan effektivt reversera antikoagulation orsakad av dabigatran, och behandling är indicerad vid svåra blödningar eller inför akut kirurgi.
Otillräcklig initial effekt eller återkommande »rekylantikoagulation« är förutsägbara fenomen kopplade till höga initiala dabigatrankoncentrationer.
Effekterna av antidottillförsel bör monitoreras genom upprepad provtagning av PK och APTT – eller hellre direkt trombintidstest (dTT).
Kvarvarande eller återkommande påverkan på dessa prov bör föranleda upprepad administrering av idarucizumab om klinisk indikation föreligger.
Under den senaste dryga 5-årsperioden har NOAK (nya orala antikoagulantia) introducerats som ett alternativ till warfarin som trombosprofylax vid förmaksflimmer och som profylax och behandling av djup ventrombos och lungemboli. Blödningar som uppkommer under pågående antikoagulationsbehandling riskerar att bli svårkontrollerade oavsett vilket preparat som använts om antikoagulationen inte reverseras. Warfarin hämmar syntesen av de K-vitaminberoende koagulationsfaktorerna och reverseras genom att de saknade koagulationsfaktorerna återförs. Detta kan ske genom tillförsel av K-vitamin vilket återställer leverns syntesförmåga, eller genom tillförsel av plasma eller faktorkoncentrat direkt till blodbanan. Vid behandling med NOAK finns ingen brist på koagulationsfaktorer, utan effekterna utövas av inhibitorsubstanser som kan hämma även exogent tillförda koagulationsfaktorer vid uppkommen blödning.
Bristen på tillförlitliga och lättillämpade metoder för att reversera effekterna av NOAK i samband med blödning eller vid behov av akut kirurgi har stimulerat till en snabb utveckling av innovativa antidoter. För dabigatran, en hämmare av trombin (FIIa) har antidoten idarucizumab funnits tillgänglig i snart 2 år. För rivaroxaban, apixaban och edoxaban, som hämmar aktiverad faktor X (FXa), är antidoten andexanet alfa för närvarande under myndighetsutredning i flera länder [1,2].
Idarucizumab
Idarucizumab är ett monoklonalt antikroppsfragment som binder till och neutraliserar dabigatran. Till skillnad från befintliga antikroppsantidoter (digitalisantidoten DigiFab och huggormsserumet ViperaTab), som är djurantikroppar utvunna ur immuniserade får, är idarucizumab en så kallad humaniserad antikropp. Detta innebär att man med rekombinant genteknik satt samman gener från möss (den antigenbindande domänen) och människa (resten) till en DNA-sekvens som i cellkultur (en »bioreaktor«) utgör mall för antikroppssyntes [3]. Idarucizumab binder dabigatran med ett stökiometriskt förhållande på 1:1 och en affinitiet som är 350 ggr högre än dabigatranets för trombin. Bindningen är närmast irreversibel och dabigatran–idarucizumabkomplexet bryts huvudsakligen ner i och utsöndras via njurarna. Idarucizumab saknar helt egeneffekt på koagulationen [1, 4]. Doseringen är 5 g (2 ampuller à 2,5 g) som ges som intravenös infusion eller långsam intravenös injektion. Idarucizumab lagerhålls i 1–2 behandlingsdoser på ett sjuttiotal svenska sjukhus som listas och uppdateras kontinuerligt i Giftinformationscentralens antidotregister (https://antidot.gic.se/antidot-web/?3).
Färre biverkningar men mera kortverkande
Användningen av antikroppar mot bakteriella toxiner (difteri, tetanus) och ormgifter var, vid sidan om vaccinerna, en central pusselbit när immunologin som vetenskap utvecklades vid Pasteurs och Kochs respektive institut i slutet av 1800-talet. Tidiga antisera, som innehöll hela IgG-antikroppar såväl som andra animaliska plasmaproteiner och celler, ledde till behandlingsframgångar men gav ofta upphov till allvarliga biverkningar som anafylaxi och serumsjuka vilket kraftigt begränsade deras kliniska användning. Dessa bieffekter har nästan helt försvunnit från moderna animaliska antikroppsantidoter som bara innehåller den antigenbindande delen av IgG (Fab) och renats från övriga reaktogena komponenter [5]. Nackdelen med moderna antikroppsantidoter är att den kraftigt minskade molekylstorleken leder till en snabbare elimination. Fab-fragmenten kan då försvinna fortare än giftet de är givna för att neutralisera. När så sker kan giftverkan återkomma genom en så kallad rekyleffekt. Detta ses vid huggormsbett där upp mot en tredjedel av patienterna som erhållit antiserum behöver en andra dos 6–12 timmar efter den första för återkommande symtom. Även idarucizumab försvinner mycket snabbt ur blodbanan, och mindre än 4 procent av toppkoncentrationen finns kvar efter 4 timmar [4].
Risk för terapisvikt vid behandling med idarucizumab
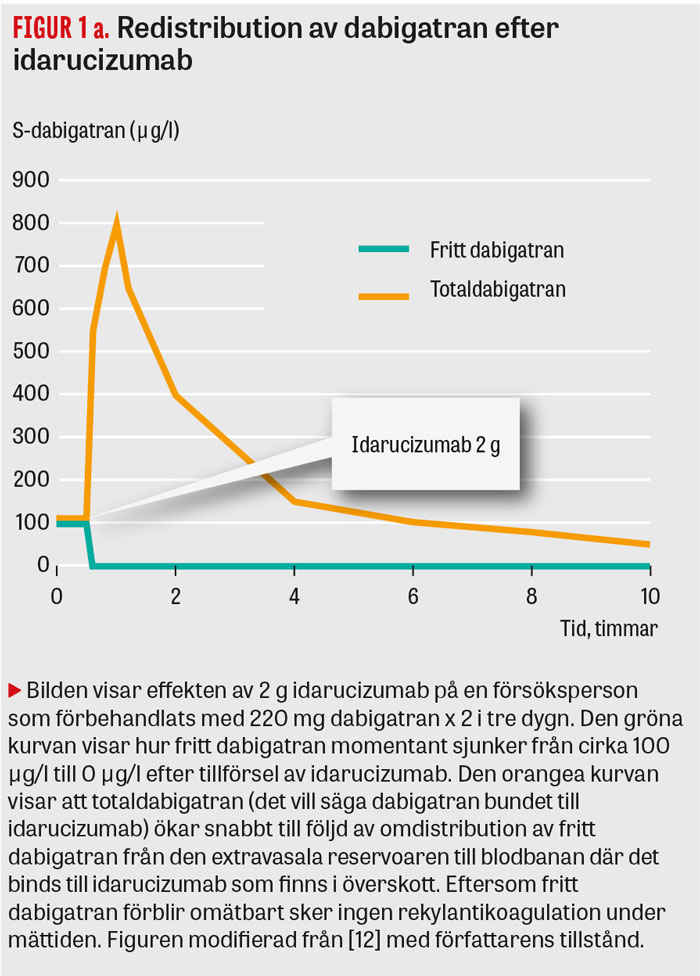
Standarddosen idarucizumab på 5 g har beräknats neutralisera allt dabigatran i kroppen vid höga normalkoncentrationer, uppmätta i en fas 3-studie av dabigatran som omfattade nästan 10 000 patienter i jämviktstillstånd [6]. Denna dos visade sig tillräcklig för att varaktigt eliminera fritt dabigatran ur blodbanan hos de flesta patienter i en publicerad interimsanalys ur den pågående fas 3-studien av idarucizumab där dabigatranbehandlade patienter med allvarliga blödningar eller behov av akut kirurgi inkluderas [1]. För en subgrupp med högre dabigatrannivåer var dosen idarucizumab dock otillräcklig för att laboratoriemässigt reversera dabigatraneffekterna. Ofullständig initial reversering förelåg hos 1/86 och »rekylantikoagulation« utvecklades hos 20 procent av patienterna under det första dygnet (3/86 4h, 6/83 12h och 16/78 24h efter idarucizumab). Förklaringen till fynden kan sammanfattas i 2 punkter (se även Figur 1 a och b):
- Antikroppsantidoter måste ges i en mängd som är tillräcklig för att neutralisera den mängd gift som finns i kroppen. Detta är förklaringen till att den pediatriska dosen av huggormsserum inte skiljer sig från vuxendosen, eftersom ormen inte gör åtskillnad mellan barn och vuxna när den biter. För idarucizumab blir storleken på dosen som krävs för att reversera antikoagulationen beroende på dabigatrannivåerna, som kan vara kraftigt förhöjda i samband med avsiktliga överdoser eller vid njursviktsorsakad ackumulation.
- Antikroppsantidoter är i stort sett begränsade till blodbanans kompartment. Detta är det kompartment där dabigatran verkar på koagulationen, och den önskade neutraliseringen blir därför blixtsnabb vid tillförsel av idarucizumab. Dabigatran har emellertid en distributionsvolym som är cirka 10 gånger större än idarucizumabs och kommer att vandra tillbaka till blodet från extravaskulära kompartment efter idarucizumabtillförsel. Om idarucizumab mättats av dabigatran eller eliminerats ur blodbanan kommer rekylantikoagulation att ske [7] .
I en djurstudie uppkom påtaglig rekylantikoagulation redan en timme efter idarucizumabtillförsel hos grisar med höga dabigatrannivåer i blodet som tillfogats ett upprepat standardiserat blödningstrauma. Grisar som inte erhöll en upprepad dos idarucizumab gick in i blödningschock, medan grisar som erhöll en andra dos idarucizumab stabiliserades [8]. Ett flertal fallrapporter publicerade under det senaste året bekräftar förekomsten av såväl otillräcklig initial reversering som rekylantikoagulation, i vissa fall med dödlig utgång [9-14].
Målstyrd antidottillförsel
För att undvika otillräcklig reversering bör effekterna av idarucizumabbehandlingen monitoreras fortlöpande och tillförsel av ytterligare antidot övervägas. Koagulationsproven PK och i synnerhet APTT påverkas vid höga terapeutiska serumnivåer av dabigatran och kan båda bli kraftigt förhöjda vid dabigatranöverdos eller ackumulation till följd av njursvikt [15]. Idarucizumabtillförsel leder, om dosen är tillräcklig, till en fullständig normalisering av PK och APTT [1]. Kvarstående eller återkommande påverkan bör tolkas som tecken på ofullständig initial reversering eller att rekyleffekt uppkommit. Normala värden av PK och APTT utesluter dock inte förekomst av låga terapeutiska serumnivåer av dabigatran, och i situationer med pågående blödningar kan faktorer andra än dabigatranpåverkan leda till påverkan på PK och APTT. För att säkert kunna bedöma graden av dabigatranpåverkan och därmed indikationen för ytterligare idarucizumabtillförsel behöver det specifika funktionella trombintidstestet dTT (Hemoclot) utföras. Detta test finns i dag emellertid bara att tillgå på ett fåtal laboratorier i landet och ofta endast under kontorstid (med undantag för Stockholmsregionen där Karolinska universitetslaboratoriet analyserar dTT [»P-dabigatran«] dygnet runt). Laboratoriemässiga tecken till kvarvarande eller återkommande dabigatranpåverkan får aldrig ensamma utgöra indikation för upprepad tillförsel av idarucizumab, men vid klinisk indikation, exempelvis hotande expansion av intrakraniell blödning, bör denna behandlingsåtgärd inte förbises.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.